


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
| A、将新制氯水滴入紫色石蕊溶液中,可以看到石蕊溶液先变红后褪色 |
| B、将新制氯水滴入硝酸银溶液中,有白色沉淀生成 |
| C、向新制氯水滴加碳酸钠溶液,有气体生成 |
| D、新制氯水应该保存在无色试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、通过甲烷的电极(X)为电池的负极,通过氧气的电极(Y)为电池正极 |
| B、放电一段时间后,电解质溶液中KOH的物质的量改变 |
| C、在标准状况下,通过5.6L氧气,完全反应后有1.0mol的电子发生转移 |
| D、放电时,通过甲烷的一极附近的pH升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
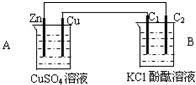 按如图装置进行实验,并回答下列问题
按如图装置进行实验,并回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁和钢材的主要化学成分相同,性质也相同 |
| B、硬铝(Al-Cu-Mg-Mn-Si合金)制成的门窗耐酸、耐碱、耐高温腐蚀 |
| C、黄铜矿(CuFeS2)可冶炼出Cu、Fe,同时可制取硫酸 |
| D、铁矿石是一种可再生资源,没有必要进行开采限制 |
查看答案和解析>>
科目:高中化学 来源: 题型:
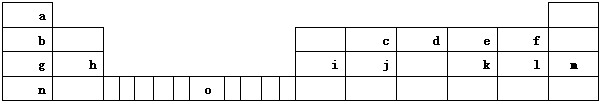
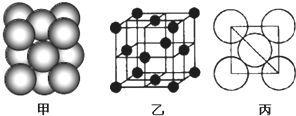
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:1 | B、2:3 |
| C、1:4 | D、1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | … | Y |
| Z | … | W |
| A、Z元素的原子半径可能比Y元素小 |
| B、Z元素的最高化合价可能比Y元素的高 |
| C、W的气态氢化物的稳定性一定比Y的强 |
| D、Z的最高价氧化物的水化物的酸性一定比W的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
238 92 |
| A、质子数为92 |
| B、电子数146 |
| C、中子数238 |
| D、元素的相对原子质量238 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com