
将一定质量的铜粉加入到100mL,某浓度的稀硝酸中充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体448mL(标准状况) 。然后向上述混合物中加入稀硫酸至不再反应为止容器剩有铜粉m2g,则m1-m2为( )
| A.5.76 | B.2.88 | C.1.44 | D.4.32 |
科目:高中化学 来源: 题型:单选题
纤维素还原法制取ClO2是将纤维素水解得到的最终产物C6H12O6与NaClO3在酸性条件下反应生成ClO2。下列叙述中正确的是
□C6H12O6+24NaClO3+12H2SO4=24ClO2↑+□CO2↑+18H2O+12Na2SO4
| A.方程式中产物CO2的计量数为6 |
| B.CO2是还原产物,ClO2是氧化产物 |
| C.氧化剂和还原剂的物质的量之比为4:1 |
| D.每生成1 mol CO2需转移24mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在KClO3+6HCl(浓)=KCl+3Cl2+3H2O的反应中,当有10 mol电子发生转移后,被氧化的氯原子与被还原的氯原子的物质的量之比是
| A.1∶5 | B.5∶1 | C.6∶1 | D.1∶6 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,在某200 mL的稀硫酸和稀硝酸的混合溶液中逐量地加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。(设硝酸只被还原为NO气体, Fe的相对原子质量为56)。下列有关分析错误的是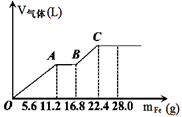
| A.原混合酸中NO3-的物质的量为0.2 mol |
| B.原混合酸中H2SO4物质的量浓度为2mol/L |
| C.OA段与BC段反应中电子转移的物质的量之比为2:1 |
| D.取20mL原混合酸加水稀释至1L后溶液的pH=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A.60 mL | B.45 mL | C. 30 mL | D. 15 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是 ( )
| A.KClO3是氧化剂 |
| B.发生氧化反应与还原反应的氯元素的质量比为5:1 |
| C.H2SO4既不是氧化剂又不是还原剂 |
| D.1mol KClO3参加反应时有10mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( )
| A.KClO3是氧化剂 |
| B.被氧化与被还原的氯元素的质量比为5:1 |
| C.H2SO4既不是氧化剂又不是还原剂 |
| D.1molKClO3参加反应时有10mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据表中信息判断,下列选项不正确的是( )
| 序列 | 参加反应的物质 | 生成物 |
| ① | KMnO4 、H2O2 、H2SO4 | K2SO4 、MnSO4…… |
| ② | Cl2 、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4- …… | Cl2 、Mn2+ …… |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是( )
| A.2Na2O2+2H2O=4NaOH+O2↑ | B.Cl2+H2O  HClO+HCl HClO+HCl |
| C.2F2+2H2O=4HF+O2 | D.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com