
| A. | 将纯水加热到95℃时,Kw变大,pH不变,水仍呈中性 | |
| B. | 向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 | |
| C. | 向纯水中加入少量氢氧化钠固体,c(H+)减小,Kw不变 | |
| D. | 向纯水中加入盐酸,将抑制水的电离,Kw变小 |
分析 A、水的电离是吸热反应,升高温度,氢离子浓度增大,pH减小;
B、一水合氨是弱碱,加入后溶液中的氢氧根浓度增大;
C、通入氯化氢后,溶液中离子浓度增大,导电能力增强;
D、硫酸氢钠是强电解质,溶于水电离出氢离子,溶液中氢离子浓度增大.
解答 解:A、△H>0,反应吸热,温度升高,平衡正向移动,溶液中氢离子浓度增大,pH降低,故A错误;
B、向水中加入稀氨水,一水合氨是弱电解质,电离的氢氧根使溶液中氢氧根浓度增大,平衡逆向移动,但是溶液中的氢氧根浓度升高,Kw不变,故B错误;
C、由于氢氧化钠是强电解质,加入后,溶液中的氢氧根离子浓度增大,平衡向逆向移动,但是溶液中的氢离子浓度减小;由于温度不变KW不变,故C正确;
D、由于HCl是强电解质,加入后,溶液中的氢离子浓度增大,平衡向逆向移动,但是溶液中的氢氧根离子浓度减小;由于温度不变KW不变,故D错误;
故选C.
点评 本题考查外界条件对弱电解质水的电离平衡的影响,注意加入酸、碱,平衡逆向移动,但是溶液中的氢离子或者氢氧根浓度反而增大,本题难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 高铁酸钠中铁显+6价 | |
| B. | 湿法中每生成1 mol Na2FeO4转移3 mol电子 | |
| C. | 干法中每生成1 mol Na2FeO4转移4 mol电子 | |
| D. | Na2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
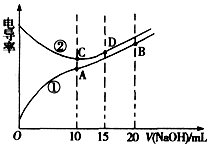
| A. | 曲线①代表滴定CH3COOH溶液的曲线 | |
| B. | A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.05 mol.L-1 | |
| C. | 在相同温度下,A、B、C三点溶液中水电离的c(H+):B<A=C | |
| D. | D点溶液中:c(Cl-)=2c(OH-)-2c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(l);△H1 2H2(g)+O2(g)=2H2O(g);△H2 | |
| B. | S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g)△H2 | |
| C. | H2(g)+Cl2(g)=2HCl(g);△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g);△H2 | |
| D. | C(s)+$\frac{1}{2}$O2(g)=CO(g);△H1 C(s)+O2(g)=CO2(g);△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Na2S2O3起始读数 | Na2S2O3 终点读数 | |
| 第一次 | 0.10mL | 18.30mL |
| 第二次 | 0.30mL | 18.30mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com