
| A. | “天宫一号”中使用的碳纤维,是一种符合材料 | |
| B. | 为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入硅胶 | |
| C. | 用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用 | |
| D. | 光导纤维是传统无机非金属材料 |
分析 A.复合材料是指以上材料中的两种或三种复合在一块儿形成的;
B.硅胶能作干燥剂,但是不能作还原剂;
C.可降解塑料是指在较短的时间内、在自然界的条件下能够自行分解成小分子的塑料;
D.传统的无机非金属材料:如水泥、耐火材料、平板玻璃、仪器玻璃和普通的光学玻璃以及日用陶瓷、卫生陶瓷、建筑陶瓷、化工陶瓷和电瓷、搪瓷、磨料(碳化硅、氧化铝)、铸石、碳素材料、非金属矿(石棉、云母、大理石等).
解答 解:A.碳纤维是由有机纤维经碳化及石墨化处理而得到的微晶石墨材料,属于新型无机非金属材料,故A错误;
B.硅胶能作干燥剂,但是不能作还原剂,所以在中秋月饼等富脂食品中放入硅胶不能防止氧化变质,故B错误;
C.用CO2合成可降解塑料-聚碳酸酯,是由许多二氧化碳小分子聚合而成的大分子,能够在较短的时间内分解,实现“碳”的循环利用,故C正确;
D.光导纤维是新型无机非金属材料,故D错误;
故选C.
点评 本题主要考查了化学与生活中有关知识,掌握它们的化学原理是解答的关键,题目难度不大,熟悉材料中的成分,能运用所学化学知识来解决实际问题.


科目:高中化学 来源: 题型:填空题
 在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值可以确定有机物分子中氢原子的种类和数目
在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值可以确定有机物分子中氢原子的种类和数目查看答案和解析>>
科目:高中化学 来源: 题型:解答题

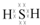 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多原子半径增大,得电子能力逐渐减弱.
;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多原子半径增大,得电子能力逐渐减弱.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3 | B. | 稀H2SO4 | C. | 稀HCl | D. | 稀HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、K+、OH-、CO32- | B. | H+、Ba2+、SO32-、Br - | ||
| C. | K+、Na+、Cl-、MnO4- | D. | Ca2+、Na+、HCO3-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②④ | C. | ②③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 反应 | 离子方程式 | 评价 |
| A | 亚硫酸钡与盐酸反应 | BaSO3+2H+═Ba2++SO2↑+H2O | 正确 |
| B B | 向NaHSO4溶液中逐滴加入Ba(OH)2至溶液呈中性 | H++SO42-+Ba2++OH-═BaSO4+H2O | 正确 |
| C C | 铝制易拉罐去膜后放入NaOH溶液中 | 2Al+2OH-═2AlO2-+H2↑ | 错误,方程式未配平 |
| D | 少量铁粉与稀硝酸反应 | 3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | 错误,少量铁粉与稀硝酸反应应生成Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向反应后的溶液中继续加入少量铁粉,铁粉可以继续溶解 | |
| B. | 氧化性:Ag+>Fe3+>Cu2+>Zn2+ | |
| C. | 反应后溶液的质量减轻 | |
| D. | 反应后溶液中Cu2+与Fe2+的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2与水反应:Na2O2+2H20═2Na++2OH-+H2↑ | |
| B. | FeSO4溶液与H2O2溶液混合:Fe2++H2O2+2H+═Fe3++2H2O | |
| C. | 向Na2SiO3溶液中通人过量的SO2:SiO32-+SO2+H2O═Na2SiO3↓+SO32- | |
| D. | NH4HCO3稀溶液与过量的Ca(OH)2溶液混合:NH4++HC03-+Ca2++2OH-═CaCO3↓+NH3•H2O+H20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com