
A.5.6 L B.11.2 L C.22.4 L D.44.8 L
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
(1)已知H—Cl键的键能为431.4 kJ·mol,下列叙述正确的是( )
A.每生成1 mol H—Cl键放出431.4 kJ能量 B.每生成1 mol H—Cl键吸收431.4 kJ能量
C.每拆开1 mol H—Cl键放出431.4 kJ能量 D.每拆开1 mol H—Cl键吸收431.4 kJ能量
(2)已知键能:H—H键为436 kJ·mol-1;H—F键为565 kJ·mol-1;H—Cl键为431 kJ·mol-1;H—Br键为366 kJ·mol-1。则下列分子受热时最稳定的是( )
A.HF B.HCl C.HBr D.H2
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)则该溶液中c(H+)_______c(OH-)(填“<”“=”或“>”),简要说明理由(用离子方程式表示)___________________________________________。
(2)现向NH4HSO3溶液中,逐滴加入少量含有酚酞的NaOH溶液,可观察到的现象是_______,写出该反应的离子方程式_______________________________;若继续滴加NaOH溶液至过量,则又发生反应的离子方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)该溶液中c(H+)____________c(OH-)(填“>”“=”或“<”),简述理由(用离子方程式表示):_______________________________________________________________。
(2)现向NH4HSO3溶液中,逐滴加入少量含有酚酞的NaOH溶液,可观察到的现象是____________;写出该反应的离子方程式:_____________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年天津市青光中学高二第一学期期末考试化学试卷 题型:填空题
(10分)已知在0.1 mol/L的NaHSO3溶液中有关微粒浓度由大到小的顺序为:
c(Na+)>c(HSO)>c(SO)>c(H2SO3)。
(1)则该溶液中c(H+)________c(OH-)(填“<”、“>”或“=”),简述理由(用离子方程式和必要的文字说明)________________ ____________________________________
____________ ________。
(2)现向NaHSO3溶液中,逐滴加入少量含有酚酞的NaOH溶液,可观察到的现象是________________________________________________________________________;
写出该反应的离子方程式_____________ _________________________
查看答案和解析>>
科目:高中化学 来源:09-10年西南师大附中高二下期期末考试化学卷 题型:填空题
(11分) 元素周期表反映了元素性质的周期性变化规律。请根据短周期元素在周期表中的位置、结构和相关性质,回答下列问题:
(1) 第VIA族元素形成的气态氢化物中沸点最高的是____________(用分子式表示),原因是____________________,该分子的空间构型为______________。
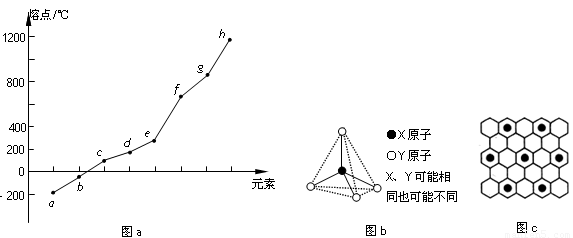
(2) 第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如表1所示,其中E的化学式为 ;第三周期元素单质的熔点(℃)变化如图a所示,其中h的元素符号为 。 (表1)
|
氢化物 |
A |
B |
HF |
D |
E |
|
沸点/℃ |
1317 |
100 |
19.5 |
|
|
(3) 第二、第三周期的某些元素能形成单质甲和化合物乙,它们具有图b所示的结构单元,甲和乙的晶体类型相同,甲的某种同素异形体与乙在高温时能发生置换反应生成h的单质和CO。若该反应生成的h的单质含有1 mol共价键,则参加反应的乙的质量为_______________g。
(4) 碳元素的某种单质具有平面层状结构,该单质的名称为__________;同一层中的原子构成许多的正六边形,单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图c所示,该物质的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com