
 ,并简要说明理由:增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大.
,并简要说明理由:增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大.| t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
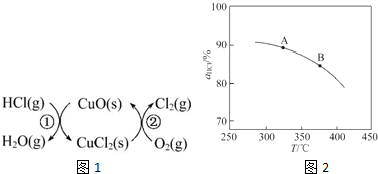
分析 (1)由图示可知,整个过程为:4HCl+O2=2Cl2+2H2O,反应②生成1molCl2(g)的反应热为△H2,则反应热化学方程式为:CuCl2(g)+$\frac{1}{2}$O2(g)=CuO(s)+Cl2(g)△H2,根据盖斯定律(①+②)×2可得总反应的热化学方程式;
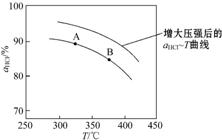
(2)①由图可知,温度越高,平衡时HCl的转化率越小,说明升高温度平衡向逆反应方向移动;
②正反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,相同温度下HCl的平衡转化率比之前实验的大;
③改变措施有利于提高αHCl,应使平衡向正反应方向移动,注意不能只增加HCl的浓度;
(3)根据v=$\frac{△n}{△t}$计算2.0~6.0min内v(Cl2),再利用速率之比等于其化学计量数之比计算v(HCl);
(4)氯气与氢氧化钙反应生成氯化钙、次氯酸钙与水.
解答 解:(1)由图示可知,整个过程为:4HCl+O2=2Cl2+2H2O,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(s)△H1,
反应②生成1molCl2(g)的反应热为△H2,则反应热化学方程式为:CuCl2(g)+$\frac{1}{2}$O2(g)=CuO(s)+Cl2(g)△H2,
根据盖斯定律(①+②)×2可得总反应的热化学方程式:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)△H=2(△H1+△H2),
故答案为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)△H=2(△H1+△H2);
(2)①由图可知,温度越高,平衡时HCl的转化率越小,说明升高温度平衡向逆反应方向移动,则正反应为放热反应,即△H<0,化学平衡常数减小,即K(A)>K(B),
故答案为:<;K(A);
②正反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,相同温度下HCl的平衡转化率比之前实验的大,故压缩体积使压强增大,画相应αHCl~T曲线的示意图为 ,
,
故答案为: ,增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大;
,增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大;
③A.增大n(HCl),HCl浓度增大,平衡右移,但HCl的转化率降低,故A错误;
B.增大n(O2),氧气浓度增大,平衡右移,HCl的转化率提高,故B正确;
C.使用更好的催化剂,加快反应速率,缩短到达平衡的时间,不影响平衡移动,HCl的转化率不变,故C错误;
D.移去生成物H2O,有利于平衡右移,HCl的转化率增大,故D正确,
故选:BD;
(3)由表中数据可知,2.0~6.0min内△n(Cl2)=(5.4-1.8)×10-3mol=3.6×10-3mol,则以Cl2的物质的量变化表示的反应速率v(Cl2)=$\frac{3.6×1{0}^{-3}}{6min-2min}$=9×10-4mol•min-1,速率之比等于其化学计量数之比,故v(HCl)=2v(Cl2)=1.8×10-3mol.min-1,
故答案为:1.8×10-3mol•min-1;
(4)氯气与氢氧化钙反应生成氯化钙、次氯酸钙与水,反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
点评 本题比较综合,为高频考点,涉及热化学方程式书写、化学平衡及平衡常数影响因素、化学反应速率的计算等,(3)中注意用单位时间内物质的量变化表示速率,较好的考查的分析解决问题的能力,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 如图表示各物质间的转化关系.已知A、H为离子化合物,H晶体中阴、阳离子的个数比为2:1,常用作干燥剂,D、E为单质.
如图表示各物质间的转化关系.已知A、H为离子化合物,H晶体中阴、阳离子的个数比为2:1,常用作干燥剂,D、E为单质.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
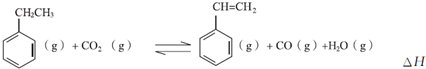
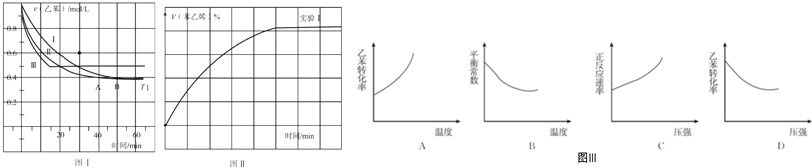

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 用品 |  |  |  |  |
| 主要成分 | H2O2 | Na2CO3 | Al(OH)3 | NaCl |
| 用途 | 消毒剂 | 发酵粉 | 抗酸药 | 调味品 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
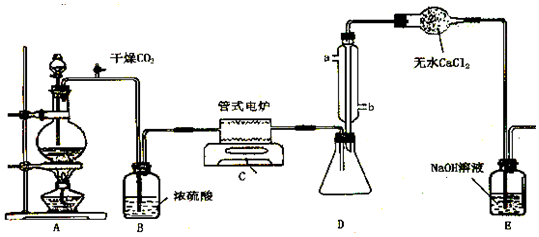
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉和油脂的水解都是高分子生成小分子的过程 | |
| B. | 2-甲基丙烷和异丁烷互为同系物 | |
| C. |  属于取代反应 属于取代反应 | |
| D. | C3H4Cl2的链状有机物的同分异构体有5种(不考虑立体异构) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CO、2mol H2 | 1mol CH3OH | 2mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α1 | α2 | α3 |
| A. | 2c1>c3 | B. | a+b=90.7 | C. | 2V2<V3 | D. | α1+α3=0.75 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com