
| A. | 硫离子的结构示意图: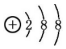 | B. | 乙烯的结构简式为CH2CH2 | ||
| C. | 过氧化氢的电子式: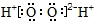 | D. | H2O分子的比例模型 |
分析 A、硫离子的核内有16个质子,核外有18个电子;
B、乙烯的结构简式中碳碳双键不能省略;
C、双氧水为共价化合物;
D、水分子为V型结构,且H原子比O原子小.
解答 解:A、硫离子的核内有16个质子,带16个正电荷,核外有18个电子,故硫离子的结构示意图为 ,故A错误;
,故A错误;
B、乙烯的结构简式中碳碳双键不能省略,故结构简式为CH2=CH2,故B错误;
C、双氧水为共价化合物,电子式为 ,故C错误;
,故C错误;
D、水分子为V型结构,且H原子比O原子小,故比例模型为 ,故D正确.
,故D正确.
故选D.
点评 本题考查了常见化学用语的书写判断,题目难度中等,涉及电子式、离子结构示意图、结构简式等知识,熟练掌握常见化学用语的表示方法为解答关键,试题培养了学生灵活应用基础知识的能力.


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
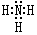 ;D可以在液态X中发生类似于与A2C的反应,写出反应的化学方程式2Na+2NH3=2NaNH2+H2↑.
;D可以在液态X中发生类似于与A2C的反应,写出反应的化学方程式2Na+2NH3=2NaNH2+H2↑.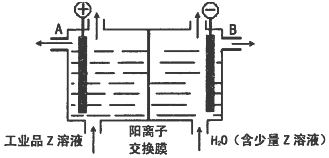
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe、MnO2 | B. | C、FeS | C. | Si、FeO | D. | CuO、Ag2S |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
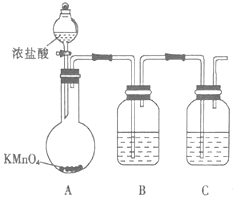

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
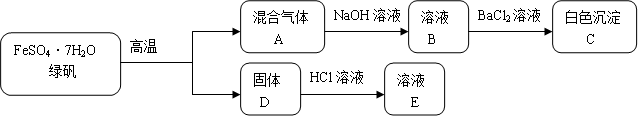
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
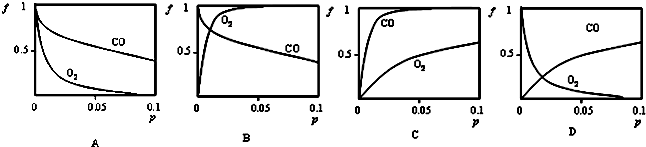

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
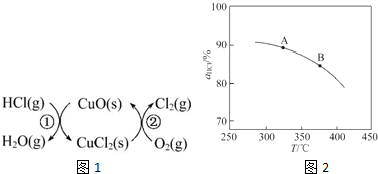
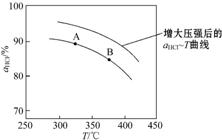 ,并简要说明理由:增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大.
,并简要说明理由:增大压强,平衡向正反应方向移动,αHCl增大,相同温度下HCl的平衡转化率比之前实验的大.| t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(Z)>r(Y)>r(M) | |
| B. | Y和M形成的化合物只含有离子键 | |
| C. | 元素非金属性由弱到强的顺序:M、N、X | |
| D. | 电解N和Z形成的化合物可得到Z的单质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com