
【题目】一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是( ) 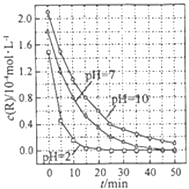
A.在0﹣50min之间,pH=2 和 pH=7 时 R 的降解百分率相等
B.溶液酸性越强,R 的降解速率越小
C.R的起始浓度越小,降解速率越大
D.在 20﹣25min之间,pH=10 时 R 的平均降解速率为 0.04molL﹣1min﹣1
【答案】A
【解析】解:A、根据图示可知:在0﹣50min之间,pH=2和pH=7时R的降解百分率都为100%,故A正确;
B、溶液酸性越强,即pH越小,线的斜率越大,可以知道R的降解速率越大,故B错误;
C、图中无法比较同一pH条件下,R的起始浓度与降解速率的关系,故C错误;
D、在 20﹣25min之间,pH=10时R的平均降解速率为 ![]() =0.04×10﹣4molL﹣1min﹣1 , 故D错误.
=0.04×10﹣4molL﹣1min﹣1 , 故D错误.
故选:A.
A、根据图中的信息可以知道在0﹣50min之间,pH=2和pH=7时R的降解百分率;
B、对比溶液的酸性强弱对R的降解速率的影响情况;
C、可以根据同一pH条件下,图示R的起始浓度与降解速率的关系来判断;
D、根据平均降解速率v= ![]() 来计算即可.
来计算即可.


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.组成糖类、油脂、蛋白质的元素都是C、H、O三种
B.葡萄糖和蔗糖不互为同分异构体,但属于同系物
C.蛋白质在碱性条件下水解为丙三醇和高级脂肪酸钠
D.“地沟油”经过加工处理后,可以用来制生物柴油和肥皂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一系列物质: NaCl、 Cl2、 NaClO、 Cl2O5、 HClO4是按某一规律排列的,下列组合中也完全照此规律排列的是( )
A. Na2CO3、C、CO2、CO、NaHCO3
B. Na2S、S、SO2、Na2SO3、Na2SO4
C. NH4Cl、N2、NaNO2、NO2、HNO3
D. P2O5、H3PO4、Na3PO4、Na2HPO4、NaH2PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元索M、N、X、Y、Z的原子序数依次增大,它们组成的单质或化合物存在如下转化关系。甲、丁为二元化合物(两种元素形成的化合物),乙、戊为单质,丙、己为三元化合物。已知25℃时,0.1mol/L的甲、丙两溶液的pH分别为l、13 ,丁、己两溶液混合时产生白色沉淀。下列推断正确的是

A. M分别与N、X、Z形成的简单化合物中,M与N形成的化合物熔点最高
B. 原子半径:Z>Y>X>M>N
C. X、Y、Z的最高价氧化物对应的水化物能相互反应
D. Z的阴离子结合质子的能力比N的阴离子强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种核素:2H、15N、18O常被用作陆地生态分析研究,下列说法正确的是( )
A.1H218O的摩尔质量为20B.2H+的核外电子数为0
C.18O的中子数为8D.15N和18O互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯水加热至较高温度,下列叙述正确的是( )
A.水的离子积变大、pH变小、呈酸性
B.水的离了积不变、pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性
D.水的离子积变大、pH变小、呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌冶炼过程中会产生大量的铅浮渣,其主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质。利用铅浮渣生产硫酸铅的流程如下。下列说法不正确的是
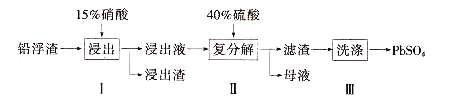
A. 步骤Ⅰ中反应的离子方程式是:Pb+4H++2NO=Pb2++2NO↑+2H2O
B. 复分解反应的方程式是:Pb(NO3)2+H2SO4= PbSO4↓+2HNO3
C. 为保证产品纯度,需控制硝酸的量以为防止Ag被溶解
D. 步骤Ⅱ得到的粗产品PbSO4 含有少量CaSO4杂质,还需用Pb(NO3)2溶液多次洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水溶液中H+和OH﹣的浓度变化曲线如图,下列说法正确的是( ) 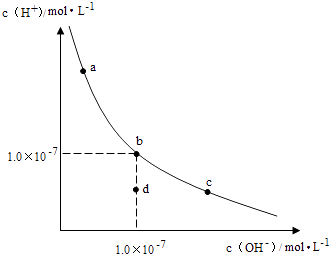
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10﹣13
C.该温度下,加入FeCl3可能引起由b向a的变化
D.该温度下,稀释溶液可能引起由c向d的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于构成细胞的化学元素的叙述,错误的是( )
A. 占细胞干重和鲜重百分比最多的元素分别是C和O
B. 不同生物细胞中的化学元素在种类上基本相同
C. C、H、O、N、P、S、K、Ca、Fe等元素为大量元素
D. 组成细胞的元素大多以化合物形式存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com