
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( ) 
A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2═6CO2+6H2O
【答案】A
【解析】解:A.根据图知,负极上C6H12O6失电子,正极上O2得电子和H+反应生成水,负极的电极反应式为C6H12O6+6H2O﹣24e﹣=6CO2+24H+ , 正极的电极反应式为O2+4e﹣+4H+═2H2O,因此CO2在负极产生,故A错误; B.葡萄糖在微生物的作用下将化学能转化为电能,形成原电池,有电流产生,所以微生物促进了反应中电子的转移,故B正确;
C.通过原电池的电极反应可知,负极区产生了H+ , 根据原电池中阳离子向正极移动,可知质子(H+)通过交换膜从负极区移向正极区,故C正确;
D.该反应属于燃料电池,燃料电池的电池反应式和燃烧反应式相同,则电池反应式为C6H12O6+6O2=6CO2+6H2O,故D正确;
故选A.
A.根据图知,负极上C6H12O6失电子,正极上O2得电子和H+反应生成水,负极的电极反应式为C6H12O6+6H2O﹣24e﹣=6CO2+24H+ , 正极的电极反应式为O2+4e﹣+4H+═2H2O;
B.葡萄糖在微生物的作用下将化学能转化为电能,形成原电池;
C.原电池中,阳离子向正极移动,所以质子通过交换膜从负极区移向正极区;
D.燃料电池反应式和燃料燃烧方程式相同.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.沸点:正戊烷>2﹣甲基丁烷>丙烷
B.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
C.相对分子质量相近的醇比烷烃沸点高是因为醇分子间存在氢键
D. 的名称为2,2,4﹣三甲基﹣4﹣戊烯
的名称为2,2,4﹣三甲基﹣4﹣戊烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是生活中的一种常见有机物,烃B分子内C、H原子个数比为1:2,核磁共振氢谱显示分子中只有一种化学环境的氢原子,D的分子式为C2H4O,各物质有如下转化关系: 
(1)A物质的官能团名称是 .
(2)甲苯生成甲的反应类型为 .
(3)D的红外光谱表明分子内除C﹣H键、C﹣C键外还含有两个C﹣O单键,D与HCl按物质的量之比1:l反应,原子利用率为100%,则D的结构简式是 .
(4)乙中有两种含氧官能团,乙与E反应的化学方程式为 .
(5)普鲁卡因的一种水解产物与甲互为同分异构体,该物质的同分异构体(包含该物质)符合下列条件的有种.(填数字)
a.分子结构中含苯环,且每个苯环有2个侧链
b.分子结构中一定含官能团﹣NH2 , 且﹣NH2直接与碳原子相连.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C60可用作储存氢气的材料,结构如右图所示.继C60后,科学家又合成了Si60、N60 , 三种物质结构相似.下列有关说法正确的是( ) 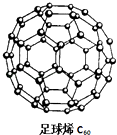
A.C60、Si60、N60都属于新型化合物
B.C60、Si60、N60分子内共用电子对数目相同
C.由于N﹣N键能小于N≡N,故N60的稳定性弱于N2
D.由于C﹣C键长小于Si﹣Si键,所以C60熔沸点低于Si60
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是周期表中前四周期的元素,其有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 负二价的A元素的氢化物在通常状况下是一种液体,其中A的质量分数为88.9% |
B | B原子得到一个电子后3p轨道全充满 |
C | C原子的p轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应生成一种常见的盐X |
D | D元素的最高化合价与最低化合价的代数和为零,其最高价氧化物为分子晶体 |
E | E的单质是日常生活中用量最大的金属材料 |
(1)元素Y是C下一周期同主族元素,比较B、Y元素第一电离能的大小I1(B)I1(Y).(填“>”或“=”或“<”)
(2)E元素原子的核外电子排布式为 .
(3)B元素最高价含氧酸一定比D元素最高价含氧酸的酸性(填“强”或“弱”).
(4)C单质分子中σ键和π键的个数比为 , C的氢化物在同族元素的氢化物中沸点出现反常,其原因是 .
(5)用高能射线照射液态H2A时,一个H2A分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式: . 写出该阳离子与硫的氢化物的水溶液反应出现黄色浑浊的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应速率的说法正确的是
A. 对于任意化学反应,其他条件不变时,增大压强都一定能加快化学反应速率
B. 相同条件下,大小相等的铝片与浓硫酸反应比与稀硫酸反应放出氢气的速率大
C. 可逆反应达到化学平衡状态时,正、逆反应的速率相等且都为0
D. 反应速率用于衡量化学反应进行的快慢,决定反应速率的主要因素是反应物的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生巨大能量,可作为航天运载火箭的推动力.下列叙述正确的是( )
A.6.02×1023个偏二甲肼分子的质量是60g
B.偏二甲肼的摩尔质量是60g
C.标况下,1mol偏二甲肼的体积为22.4L
D.6g偏二甲肼中电子数目为6NA(NA表示阿伏伽德罗常数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①Cl2+2KBr=2KCl+Br2 , ②KClO3+6HCl=3Cl2+KCl+3H2O,③2KBrO3+Cl2=Br2+2KClO3 , 下列说法正确的是( )
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C.反应②中还原剂与氧化剂的物质的量之比为6:1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列九种物质:①H2②Cu ③CuO ④CO2⑤稀H2SO4⑥稀硝酸 ⑦氨水 ⑧Ba(OH)2固体 ⑨熔融Al2(SO4)3 , 请回答下列问题.(前3个小题填写物质的序号)
(1)上述物质中,属于强碱的是;
(2)上述物质中,在该状态下既是电解质又能导电的是;
(3)上述物质或溶液中若两两反应的离子方程式为:H++OH﹣═H2O则,对应的两种物质是;
(4)上述两种物质的组合后在一定条件下能发生置换反应,请写出其化学方程式是;
(5)在⑧的溶液中通入少量的④,请写出该反应的离子方程式: .
(6)在特殊条件下,金属Al与⑥发生反应的化学方程式为:8Al+30HNO3═8Al(NO3)3+3X+9H2O,该反应中生成的X是一种盐,其化学式为 , 其中还原剂与氧化剂的物质的量之比是 , 当有8.1g Al发生反应时,转移电子的数目为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com