
有两条途径可以使重晶石(BaSO4)转化为碳酸钡,如下图所示:
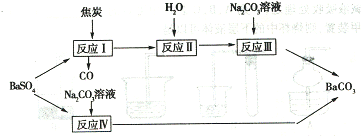
试回答下列问题:
(l)反应I 中发生的主要反应为:BaSO4 + 4C = BaS + 4CO ,若1 mol BaSO4 完全反应,电子转移的物质的量为 ;
(2)Na2CO3 溶液的pH 大于10 ,用离子方程式说明其主要原因 ,其溶液中离子浓度由大到小的顺序是 ;
(3)已知反应IV 中发生的反应为:BaSO4 ( s ) + CO3 2- ![]() BaCO3 ( s ) + SO42- ,写出此反应平衡常数表达式K = ;若KSP (BaSO4)为
BaCO3 ( s ) + SO42- ,写出此反应平衡常数表达式K = ;若KSP (BaSO4)为![]()
![]() ,KSP (BaCO3)为
,KSP (BaCO3)为![]() ,则K 的值为 ;
,则K 的值为 ;
(4)若每次加入1L 2mol · L-1的Na2CO3溶液,至少需要 次可以将0.2mol BaSO4转化为BaCO3 。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解

| 16a |
| 22.4b |
| 16a |
| 22.4b |
| 高温高压 |
| 催化剂 |
| 高温高压 |
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可以通过三条途径按不同要求来制取氮:
①加热条件下用NH3还原CuO制得纯净的N2和活性铜粉;
②将空气通过灼热的活性铜粉制得较纯净的N2;
③加热NaNO2(一种致癌物质,有剧毒)与NH4Cl的混合浓溶液制取N2。
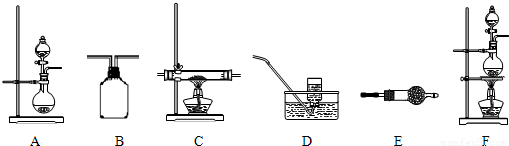
如图所示,给出了按上述途径制N2的可供选择的几种实验仪器,其他必要的仪器如铁架台、铁夹、铁圈、石棉网、酒精灯等未列出。

(1)按途径①制取N2时所需的氨气要用浓氨水与生石灰作原料制取,最好要用上述仪器中的 (填仪器代码,下同)作为氨气发生装置,该反应的化学方程式为 。要制取并收集纯净的N2(允许含少量的水范气),还应使用到上述仪器中的 (按气流从左到右的顺序列出)。
(2)按途径②制取N2,原料气空气是通过向 (填上述仪器代码)中加入
而送入反应器的,反应器内发生的现象是 。
(3)上述三种制取N2的途径,①和②两条途径常常被协同使用而越来越受到人们的关注,这种方法与途径③相比其优越性在于 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年湖南省邵阳市邵阳县石齐学校高二(下)期末化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com