
����Ŀ����֪�ǽ���������S���ǵ���ɫ�����ĩ��������ˮ��Ϊ����֤��Ԫ�صķǽ����Ա���Ԫ�صķǽ�����ǿ��ij��ѧʵ��С�����������ʵ�飬��ش��������⣺

��1��װ��A�ķ�Һ©����ʢװ���Լ��� ����ƿ�м�����Լ��� ��
��2�����߿��ڵ�ʵ��װ�õ����� ��
��3��װ��B��ʢ�ŵ��Լ��� ��ѡ�����������Լ��Ĵ��룩��ʵ������Ϊ ����ѧ��Ӧ����ʽ�� ���÷�Ӧ�������ֻ�����Ӧ�����е� _______��Ӧ��
A��Na2S��Һ B��Na2SO3��Һ C��Na2SO4��Һ
��4��������Щ��ʵ�ܹ�˵����Ԫ�صķǽ����Ա���Ԫ�صķǽ�����ǿ���Ծ�һ������
���𰸡���1��Ũ���� �������̣�2����ȥCl2�л��е��Ȼ��� ��3��A ��Һ����ǻ���dz��ɫ�������� Cl2+Na2S=2NaCl+S�� �û���4��3Cl2+2Fe=2FeCl3 S+Fe="FeS" �����HCl��H2S�ȶ���
�������������������1��Ϊ����֤��Ԫ�صķǽ����Ա���Ԫ��ǿ�����õ������������Ƶķ�Ӧ�����װ��A����ȡ������װ�ã���װ��A�з�Һ©����ʢװ���Լ�ΪŨ���ᣬ����ƿ�м�����Լ��Ƕ������̣�
��2�������Ƶõ������к���HCl���ʣ�������߿��ڵ�ʵ��װ�õ������dz�ȥ��ȥCl2�л��е��Ȼ��⣻
��3��װ��B����������֤��Ԫ�صķǽ����Ա���Ԫ��ǿ�����װ��B��ʢ�ŵ��Լ���Na2S��Һ��ʵ����������Һ����ǻ���dz��ɫ���������������ķ�Ӧ�Ļ�ѧ����ʽΪ��Cl2+Na2S=2NaCl+S�����÷�Ӧ�����û���Ӧ��
��4���ܹ�֤����Ԫ�صķǽ����Ա���Ԫ��ǿ��ʵ����ʵ�У�Cl2��S��������H2������Ӧ��HCl��H2S�ȶ���Cl2�ܰ�Fe������+3��̬����Sֻ�ܰ�Fe������+2��̬�ȵȡ�


 ������ϵ�д�
������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��8���л��������ת����ϵ��
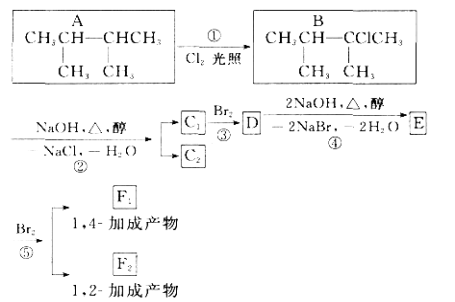
��ش��������⣺
��1��������ͼ�У�����________��Ӧ������________��Ӧ(�Ӧ����)��
��2��������E����Ҫ�Ĺ�ҵԭ�ϣ�д����D����E�Ļ�ѧ����ʽ��_______________________________________________________________��
��3�� C 1�Ľṹ��ʽ��______________________��F 1�Ľṹ��ʽ��_____________________________��
��4�� ����8�ֻ������У����ڶ�ϩ������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪŨ������ͭƬ��Ӧ��װ�á���ش�
��1��Ũ������ͭƬ��Ӧ�Ļ�ѧ����ʽΪ ��

��2����Ӧһ��ʱ����Թ�����Ʒ����Һ�������� ��
��3�������йظ�ʵ���˵���У�����ȷ���� ��
A���÷�Ӧ��Ũ����ֻ��������
B���Թ����к��м�Һ�����������������չ�����SO2����ֹ������Ⱦ
C����Ӧһ��ʱ����Թܼ��е���Һ��������ʢ��ˮ���ձ�����Һ����ɫ
D����0��04mol���ʵ�Ũ������������ͭƬ��Ӧ�����ռ���448mL��SO2����״����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������, ��ѧ��������һ�����͵��Ҵ���أ�DEFC��, ���û������������ܼ�, ��200������ʱ����, �Ҵ���رȼ״����Ч�ʸ߳�32���Ҹ��Ӱ�ȫ������ܷ�ӦʽΪ: C2H5OH+3O2 ![]() 2CO2+3H2O������˵������ȷ����
2CO2+3H2O������˵������ȷ����
A��C2H5OH�ڵ�صĸ����ϲμӷ�Ӧ B��1 mol�Ҵ�������ת��6 mol����
C�������·�е����ɸ����ص����������� D����������õ��ӵ�������O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Դ��Ҳ����Ҫ�Ļ���ԭ�ϣ����������������ⷽ�����������������
��1������һ��H2S�ȷֽⷨ����ӦʽΪ��2H2S(g)![]() 2H2(g)+S2(g)��H
2H2(g)+S2(g)��H
�ں����ܱ����������ⶨH2S�ֽ��ת����(H2S����ʼŨ�Ⱦ�Ϊcmol/L)���ⶨ�������ͼ��ͼ������a��ʾH2S��ƽ��ת�������¶ȹ�ϵ�����߱�ʾ��ͬ�¶�����Ӧ������ͬʱ��δ�ﵽ��ѧƽ��ʱH2S��ת���ʡ�

�١�H______0��(������������������=��)��
����985��ʱ����Ӧ��tmin�ﵽƽ�⣬��ʱH2S��ת����Ϊ40%����tmin�ڷ�Ӧ����v(H2)=______(�ú�c��t�Ĵ���ʽ��ʾ)��
����˵�����¶ȵ����ߣ�����b������a������ԭ��______��
��2������������CaOΪ�����壬���������(��C��)��ˮ������Ӧ��ȡH2�������Ҫ��Ӧ������
I��C(s)+H2O(g)�TCO(g)+H2(g) ��H=+131.0kJ/mol
����CO(g)+H2O(g)�TCO2(g)+H2(g) ��H=-43kJ/mol
����CaO(s)+CO2(g)�TCaCO3(s) ��H=-178.3kJ/mol
��������ӦC(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g)����H=______��
CaCO3(s)+2H2(g)����H=______��
��K1��K2��K3�ֱ�Ϊ��ӦI����������ƽ�ⳣ������ƽ�ⳣ��K=_____________(��K1��K2��K3��ʾ)��
�����ڿ��淴ӦC(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g)����ȡ���´�ʩ�������H2��������______��(����ĸ���)
CaCO3(s)+2H2(g)����ȡ���´�ʩ�������H2��������______��(����ĸ���)
A��������ϵ���¶�
B��ѹ�����������
C���ʵ�����ˮ������ͨ����
D������CaO����
����ͼΪ��ӦI��һ���¶��£�ƽ��ʱ����������ٷֺ�����ѹǿ�仯�Ĺ�ϵͼ������Ӧ��ijһƽ��״̬ʱ�����c(H2O)=2c(H2)=2c(CO)=2mol/L���Ը���H2O������ٷֺ����仯���ߣ���������CO�ı仯����ʾ��ͼ��
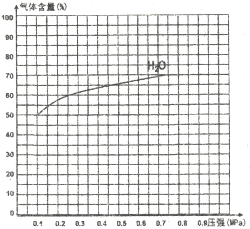
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Īɳ������һ����ʹҩ�����ĺϳ�·�����£�
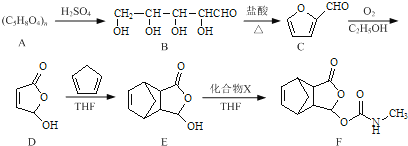
��1��B������̼ԭ����Ϊ____________��������D�к��������ŵ�����Ϊ____________��
��2��C������������ͭ��Ӧ�Ļ�ѧ����ʽΪ____________��
��3��д��ͬʱ��������������E��һ��ͬ���칹��Ľṹ��ʽ��____________
I���˴Ź���������4���壻
�����ܷ���������Ӧ��ˮ�ⷴӦ��
��������FeCl3��Һ������ɫ��Ӧ��
��4����֪E+X��FΪ�ӳɷ�Ӧ��������X�Ľṹ��ʽΪ____________��
��5����֪��![]() ��������
�������� �Ǻϳɿ�����ҩ������Τ���м��壬����ƺ���������
�Ǻϳɿ�����ҩ������Τ���м��壬����ƺ���������![]() ��
��![]() Ϊԭ�Ϻϳɸû�����(�úϳ�·������ͼ��ʾ����ע����Ӧ����)���ϳ�·������ͼʾ�����£�
Ϊԭ�Ϻϳɸû�����(�úϳ�·������ͼ��ʾ����ע����Ӧ����)���ϳ�·������ͼʾ�����£�![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѧ��ѡ��2 ��ѧ�뼼����
��.�����й�������ȷ����( )
A.����п�̵����,MnO2�Ǵ���
B.��пŦ�۵�ع���ʱ,Ag2O����ԭΪAg
C.�ŵ�ʱ,Ǧ������������Ũ�Ȳ�������
D.���ʱ,���ƵĽ�����Ʒ���淢����ԭ��Ӧ
��.п��һ��Ӧ�ù㷺�Ľ���,Ŀǰ��ҵ����Ҫ���á�ʪ��������ұ��п,ij��п�����Ҫ�ɷ�ΪZnS(��������FeS�������ɷ�),����Ϊԭ��ұ��п�Ĺ���������ͼ��ʾ:

�ش���������:
��1����п����ı������������յķ���¯�н���,��������ɰ����Ҫ�ɷֵĻ�ѧʽΪ ��
��2�����չ����в����ĺ��������ɾ�������,��������ں����� ������
��3������Һ�������������м������Ҫ����Ϊ ,�������� ��
��4�������������е�������������,��������Pb-Ag�Ͻ���Ե缫,�����ݳ������� ��
��5���Ľ���пұ������,�����ˡ���ѹ�������ȫʪ������,��ʡ�������¿�����Ⱦ�ı��չ���,�ֿɻ��һ���й�ҵ��ֵ�ķǽ������ʡ�����ѹ������з�����Ҫ��Ӧ�����ӷ���ʽΪ ��
��6���ҹ��Ŵ������á�������ұ��п,������Ӧ�����ġ��칤������й��ڡ�������Ǧ���ļ���:��¯��ʯʮ��,װ����һ�����,����,Ȼ�������ú̿����ʢ,�����н,�����Ѻ�,����,���,�ٹ�ȡ��,����,����ǦҲ��������п���չ�����Ҫ��Ӧ�Ļ�ѧ����ʽΪ ��(ע:¯��ʯ����Ҫ�ɷ�Ϊ̼��п,��Ǧ��ָ����п)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���飨As���ǵ������ڵ�VA��Ԫ�أ�������Ȼ���еĺ������ߣ���������ʶ�����о�������ʷȴ�ܳ���
(1)��֪H3AsO3������ƫ���ԵĻ����H3AsO3��As�Ļ��ϼ�Ϊ_____�������������ᷴӦʱ�����εĻ�ѧʽΪ_______________��Na2HAsO3��Һ�ʼ��ԣ�ԭ����_________________�������ӷ���ʽ��ʾ��������Һ��c��H2AsO3-�� _____c��AsO33-�����>������<����=������
��2��������Ȼ������Ҫ��������ʽ�����ۻ�As4S4���ƻ�As2S3�ȣ����ڡ�
�ٹ�ҵ�����ۻ�Ϊԭ���Ʊ��顢������˪��As2O3����ԭ������ͼ��

��Ӧa�����ķ���ֱ���ŷſ��ܴ����Ļ���������__________ _____����д����Ӧb�Ļ�ѧ����ʽ��_________________________��
�ڴƻƿɱ�Ũ��������ΪH3AsO4��S�����ᱻ��ԭΪNO2����Ӧ�л�ԭ�������������ʵ���֮��Ϊ_________��
����c��As3+��=0.01mol/L�Ĺ�ҵ��ˮ�м���FeS����������ǡ����ȫ��ȥ��С��1��10-5mol/L�������ʱc��Fe2+��=_____mol/L������֪Ksp��As2S3��=1��10-22��Ksp��FeS��=6��10-18��
��3��ijԭ���װ������ͼ������ܷ�ӦΪAsO43-+2I��+H2O![]() AsO33-+I2+2OH����P������Һ����ɫ�����ɫʱ�������ϵĵ缫��ӦʽΪ_______________����������ָ����к���Q���м���һ������NaOH���������_____���P����Q������������
AsO33-+I2+2OH����P������Һ����ɫ�����ɫʱ�������ϵĵ缫��ӦʽΪ_______________����������ָ����к���Q���м���һ������NaOH���������_____���P����Q������������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ú�ͭ�����Ĵ�п�Ʊ�����п��������ʡ���������ͼ���й��������£�

���� | Cu(OH)2 | Zn(OH)2 | Fe(OH)3 | ZnS | CuS |
Ksp | 5.0��10��20 | 2.0��10��16 | 4.0��10��38 | 1.2��10��23 | 8.5��10��45 |
��ش��������⣺
��1����п�е�ͭ������ϡ��Һ��Ӧ�Ļ�ѧ����ʽΪ__________________________��ͼ�д�������XҪ�ܹ�������ɫ��ѧ˼�룬���貹������______���ѧʽ����
��2������ҺI��c(Cu2��)Ϊ0.05mol��L��1������ҺII��c(Fe3��)��____mol��L��1��
��3��������A��Zn��ȡ9.61 g����C�ܽ���������500mL 2 mol��L��1ϡ�����У����ռ�����״����2.24L�����壬��������Һ�м���2 mol��L��1NaOH��Һ�������ɳ������ʱ������������Ϊ_____g��������A����һ�����ʣ�ȡ���ֹ���C���Թ��У�������������г�����ζ���壬��÷�Ӧ�����ӷ���ʽΪ________________________��
��4����Һ������Ũ����____________�����ˡ�ϴ�ӡ�������õ��ϴ���������п���壻��Һ�������Ʊ�ZnS��ʵ��ѡ����ǣ�NH4��2S��Һ������Na2S��Һ��Ϊ��Ӧ������Ǻ����Ƶõ�ZnS���н϶�����ʣ����������____________���ѧʽ����
��5������п���������Ըɵ�صĸ������ɵ�ز�ʹ��ʱ�����ڸ�����������Һ�Ӵ��������Էŵ練Ӧ��2NH4����Zn��2NH3��H2����Zn2������ɵ����Զ����١�д��Ǧ���ز�ʹ��ʱ���������Ϸ����Էŵ�Ļ�ѧ����ʽ__________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com