
【题目】t℃时,AgX(X=Cl、Br)的溶度积与c(Ag+)和c(X-)的相互关系如下图所示,其中A线表示AgCl,B线表示AgBr,已知p(Ag+)=-lgc(Ag+),p(X-)=-lgc(X-)。下列说法正确的是( )

A. c点可表示AgCl的不饱和溶液
B. b点的AgCl溶液加入AgNO3晶体可以变成a点
C. t℃时,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)平衡常数K=10-4
AgBr(s)+Cl-(aq)平衡常数K=10-4
D. t℃时,取a点的AgCl溶液和b点AgBr溶液等体积混合,会析出AgBr沉淀
【答案】D
【解析】
根据图示,A为氯化银溶液中p(Ag+)与p(Cl-)的关系曲线,线上每一点均为氯化银的饱和溶液,如a点,p(Ag+)=-lgc(Ag+)=5,则c(Ag+)=10-5 mol/L,p(Cl-)=-lgc(Cl-)=5,则c(Cl-)=10-5 mol/L,则Ksp(AgC1)= c(Ag+)×c(Cl-)=10-5×10-5=10-10,同理Ksp(AgBr)=c(Ag+)c(Br-)=10-7×10-7=10-14。A. c点,c(Ag+)=10-4 mol/L,c(Cl-)=10-4 mol/L,因为10-4×10-4=10-8>Ksp(AgC1)=10-10,说明是AgC1的过饱和溶液,故A错误;B. b点的AgC1溶液加入AgNO3晶体,c(Ag+)增大,但c(Cl-)基本不变,不能变成a点,故B错误;C. t℃时,AgC1(s)+Br-(aq)![]() AgBr(s)+C1-(aq)平衡常数K=
AgBr(s)+C1-(aq)平衡常数K=![]() =
=![]() =
=![]() =104,故C错误;D. t℃时,取a点的AgC1溶液和b点AgBr溶液等体积混合,c(Ag+)=
=104,故C错误;D. t℃时,取a点的AgC1溶液和b点AgBr溶液等体积混合,c(Ag+)=![]() ×10-4 mol/L +
×10-4 mol/L +![]() ×10-7 mol/L≈
×10-7 mol/L≈![]() ×10-4mol/L,c(Br-)=
×10-4mol/L,c(Br-)=![]() ×10-7 mol/L,则c(Ag+)c(Br-)=
×10-7 mol/L,则c(Ag+)c(Br-)=![]() ×10-4×
×10-4×![]() ×10-7>10-14,有AgBr沉淀生成,故D正确;故选D。
×10-7>10-14,有AgBr沉淀生成,故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】以苯为基础原料,可以合成多种有机物。

已知:I.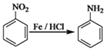
II.![]()
回答下列问题:
(1)由苯合成有机物A用到的无机试剂为______________。
(2)B分子中的官能团的名称为_________,B→C的反应类型为_______________。
(3)生成PF树脂的化学方程式为_____________。
(4)试剂D是___________________(填代号)。
a.溴水 b.高锰酸钾溶液 c.Ag(NH3)2OH溶液 d.新制Cu(OH)2悬浊液
(5)写出同时满足下列条件的肉桂酸乙酯的一种同分异构体________________。
①苯环上仅有2个取代基且处于对位
②能发生水解反应和银镜反应,其中一种水解产物遇FeCl3溶液显紫色
③为顺式异构
(6)以乙醇为原料合成CH3-CH=CH-COOCH2CH3,其他试剂任选,写出合成路线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一无色溶液,其中可能含有 Fe3+、Al2+ 、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其探作和有关现象如下图所示:
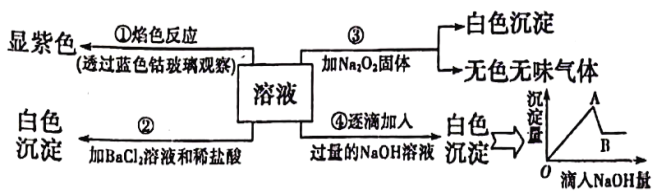
请你根据上图推断:
(1)原溶液中一定存在的阴离子有(写化学式):_________________________。
(2)写出实验④中产生的沉淀有:______________________。
写出由A→B过程中所发生反应的离子方程式: ______________________。
(3)实验③中产生无色无味气体所发生的化学方程式为:______________________。
(4)实验②中加入稀盐酸的目的是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置及操作均正确的是

A. 图I中A盛放碳酸氢钠,B盛放碳酸钠,可对比二者的热稳定性
B. 图II可用于从NaCl溶液中提取NaCl晶体
C. 图III为实验室制备氨气的实验药品与发生装置
D. 图IV为实验室制备观察氢氧化亚铁的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上氟气可作为火箭燃料中的氧化剂。1886年法国化学家H.M0issan通过电解氟氢化钾(KHF2)的氟化氢无水溶液第一次制得氟气。已知:KF+HF=KHF2,制备氟气的电解装置如图所示。下列说法错误的是
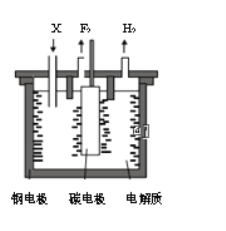
A. 钢电极与电源的负极相连
B. 电解过程需不断补充的X是KF
C. 阴极室与阳极室必须隔开
D. 氟氢化钾在氟化氢中可以电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e均为周期表前四周期元素,原子序数依次增大,相关信息如下表所示。
a | 原子核外电子分别占3个不同能级,且每个能级上排布的电子数相同 |
b | 基态原子的p轨道电子数比s轨道电子数少1 |
c | 在周期表所列元素中电负性最大 |
d | 位于周期表中第4纵行 |
e | 基态原子M层全充满,N层只有一个电子 |
请回答:
(1)d属于______区的元素,其基态原子的价电子排布图为_____________。
(2)b与其同周期相邻元素第一电离能由大到小的顺序为__________(用元素符号表示)。
(3)c的氢化物水溶液中存在的氢键有________种,任意画出一种_________。
(4)a与其相邻同主族元素的最高价氧化物的熔点高低顺序为___________(用化学式表示)。若将a元素最高价氧化物水化物对应的正盐酸根离子表示为A,则A的空间构型为____________;A的中心原子的轨道杂化类型为______________,与A互为等电子体的一种分子为____________(填化学式)。
(5)e与Au的合金可形成面心立方最密堆积的晶体,在晶胞中e原子处于面心,该晶体具有储氢功能,氢原子可进入到由e原子与Au原子构成的四面体空隙中,储氢后的晶胞结构与金刚石晶胞结构相似,该晶体储氢后的化学式为______________,若该晶体的相对分子质量为M,密度为a g/cm3,则晶胞的体积为________(用NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体能表明②中木炭与浓硝酸发生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,不一定说明木炭与浓硝酸发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行)。
![]()
(1)若B的溶液显黄色,一定条件下B的饱和溶液可与沸水反应生成红褐色分散系
①实验室制A单质的反应的离子方程式_______________________________________;
A单质的常用检验方法____________________________
②C溶液中加入氢氧化钠溶液的现象_________________________________________;
③一定条件下W与水反应的化学方程式_______________________________________;
(2)若W为NaOH,且B为白色沉淀
①C的化学名称为______________;
②W与某金属单质也可生成C,该反应的离子方程式______________________________;
③B与W反应生成C的离子反应方程式________________________________________;
(3)若B能使品红褪色,加热又变红,C能与水反应生成一种强酸
①B转化为C的化学方程式_________________________________________________
②若A是一种化合物,A与B反应的化学方程式__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. CO、CO2、NO、NO2都是大气污染气体,在空气中都能稳定存在
B. 焰色反应、离子反应中都一定存在化学反应
C. 明矾溶于水能产生具有吸附性的胶体粒子,可作漂白剂
D. 可用浓盐酸检验输送氨气的管道是否漏气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com