
【题目】下列说法正确的是( )
A. 根据反应Cu+H2SO4![]() CuSO4+H2↑可推知Cu的还原性比H2的强
CuSO4+H2↑可推知Cu的还原性比H2的强
B. 在反应CaH2+2H2O===Ca(OH)2+2H2↑中,水作氧化剂
C. 反应3NO2+H2O===2HNO3+NO中氧化剂和还原剂的物质的量之比是3∶1
D. Cl2的氧化性强于I2的氧化性,故置换反应I2+2NaClO3===2NaIO3+Cl2不能发生
科目:高中化学 来源: 题型:
【题目】(1)含有相同分子数的SO2、SO3气体,同温同压下,体积之比为_________,物质的量之比为__________,物质的质量之比为____________,氧原子的个数之比为________。
(2)足量的金属Al与200mL3mol/L盐酸完全反应,生成标准状况下的氢气体积为_________L。反应中消耗的铝为_________g,该反应转移的电子数目为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只用一种试剂,将NH4Cl、(NH4)2SO4、NaCl、Na2SO4四瓶溶液区分开,这种试剂是( )
A. NaOH溶液 B. AgNO3溶液
C. BaCl2溶液 D. Ba(OH)2浓溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z。反应2min 后,测得参加反应的X2为0.6mol/L,用Y2的变化表示的反应速率v(Y2) =0.1mol/(L·min),生成的c(Z)为0.4mol/L,则该反应的化学方程式是
A. X2+2Y2 ![]() 2XY2 B. 2X2+Y2
2XY2 B. 2X2+Y2![]() 2X2Y
2X2Y
C. 3X2+Y2![]() 2X3Y D. X2+3Y2
2X3Y D. X2+3Y2![]() 2XY3
2XY3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学欲探究SO2的性质,并测定空气中SO2的含量。他们设计如下实验装置(如图),请你参与探究,并回答问题:

(1)装置中的氨水可吸收多余的SO2,发生反应的离子方程式是___________,使用倒立的漏斗能防止倒吸的原因是________________。
(2)装置B用于检验SO2的漂白性,其中所盛试剂为__________,装置D用于检验SO2的_____性质;
(3)装置C中发生的现象是_______________;
(4)如果用硫酸和亚硫酸钠反应制取二氧化硫,装置如图所示。其中a导管的作用是___________________,所用硫酸为70%浓硫酸,不用稀硫酸原因是______________。

(5)他们拟用以下方法(如图)测定空气中SO2含量(假设空气中无其他还原性气体)。
方案1:
① 洗气瓶C中溶液蓝色消失后,若没有及时关闭活塞A,则测得的SO2含量______(填“偏高”、“偏低”或“无影响”)。
方案Ⅱ:

② 实验中若通过的空气的体积为33.6L(已换算成标准状况),最终所得固体质量为0.233g,试通过计算确定该空气中二氧化硫的含量是否合格(计算过程): ____________。(空气中二氧化硫的体积分数小于0.05%表示合格)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将m g钠和铝的混合物放入n g足量水中,待反应停止后,得到a g沉淀,则滤液中的溶质是( )
A. NaAlO2 B. NaAlO2和NaOH C. Al(OH)3 D. NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红珊瑚栖息于200~2000 m的海域,产于台湾海峡、南中国海,它与琥珀、珍珠被统称为有机宝石。在中国,珊瑚是吉祥的象征,一直用来制作珍贵的工艺品。红珊瑚是无数珊瑚虫分泌的石灰质大量堆积形成的干支状物,其红色是因为在海底长期积淀某种元素,该元素是( )
A. Na B. Fe C. Si D. Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:
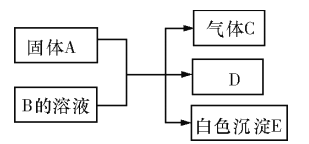
(1)若A是短周期中原子半径最大的元素构成的单质,E 既可溶于盐酸又可溶于NaOH ,E 溶于NaOH 溶液的离子方程式为___________;工业上冶炼A 的化学反应方程式为_________________。
(2)若A为红色金属,B 为某酸的浓溶液,C 为可形成酸雨的无色气体。则A 与B反应的化学方程式为___________________________。
(3)若B为某酸式盐的溶液,C 是既含有极性键又含有非极性键的四原子分子,则实验室制取C的化学方程式为 _________________;0.1molC 完全燃烧生成液态水时放热130kJ·mol-1,则表达C 燃烧热的热化学方程式是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com