
【题目】下表是元素周期表的一部分:

针对表中的①~⑩号元素,用元素符号或化学式填空:
(1)在这些元素中,最易得电子的元素是____,失电子能力最强的元素是________。
(2)化学性质最不活泼的元素是____,其原子结构示意图为________。
(3)④、⑨的最高价氧化物对应的水化物在溶液中反应的离子方程式是________。
(4)在①②③④四种元素,原子半径由大到小的顺序是________。
(5)元素⑥、⑦、⑩的最高价氧化物对应的水化物中,酸性最强的是____。
【答案】 F K Ar 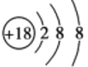 Al(OH)3+OH-=AlO2-+2H2O Mg>Al>N>F H2SO4
Al(OH)3+OH-=AlO2-+2H2O Mg>Al>N>F H2SO4
【解析】由元素在周期表中的位置可以知道,①为N、②为F、③为Mg、④为Al、⑤为Si、⑥为P、⑦为S、⑧为Ar、⑨为K、⑩为Se。
(1)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,金属性越强,越容易失去电子;
(2)稀有气体Ar的化学性质最不活泼,其原子核外有18个电子,有3个电子层,各层电子数为2、8、8;
(3)氢氧化铝是两性氢氧化物,与氢氧化钾反应生成偏铝酸钾与水;
(4)同周期自左而右原子半径减小,同主族自上而下原子半径增大;
(5)同主族自上而下非金属性减弱,最高价含氧酸的酸性减弱。
详解:由元素在周期表中的位置可以知道,①为N、②为F、③为Mg、④为Al、⑤为Si、⑥为P、⑦为S、⑧为Ar、⑨为K、⑩为Se。
(1)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,上述元素中K的金属性最强,K最容易失去电子,上述元素中F的非金属性最强,
因此,本题正确答案是:F;K;
(2)稀有气体Ar的化学性质最不活泼,其原子核外有18个电子,有3个电子层,各层电子数为2、8、8,原子结构示意图为: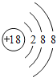 ,
,
因此,本题正确答案是:Ar; ;
;
(3)氢氧化铝是两性氢氧化物,与氢氧化钾反应生成偏铝酸钾与水,反应离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,
因此,本题正确答案是:Al(OH)3+OH-=AlO2-+2H2O;
(4)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径: Mg>Al>N>F,
因此,本题正确答案是:Mg>Al>N>F;
(5) P、S同周期,自左向右非金属性增强,非金属性越强最高价含氧酸的酸性越强,酸性H2SO4大于H3PO4;S、Se同主族,自上而下非金属性减弱,非金属性越强最高价含氧酸的酸性越强,酸性H2SO4大于H2SeO4,故H2SO4的酸性最强,
因此,本题正确答案是:H2SO4。


科目:高中化学 来源: 题型:
【题目】可逆反应:mA(g)+nB(g)![]() pC(g)+gD(g)的v-t图象如图甲所示。若其他条件都不变,只在反应前加入合适的催化剂,则其v-t图象如图乙所示。现有下列叙述:①a1=a2;②a1<a2;③b1=b2;④b1<b2;⑤t1>t2;⑥t1=t2。
pC(g)+gD(g)的v-t图象如图甲所示。若其他条件都不变,只在反应前加入合适的催化剂,则其v-t图象如图乙所示。现有下列叙述:①a1=a2;②a1<a2;③b1=b2;④b1<b2;⑤t1>t2;⑥t1=t2。
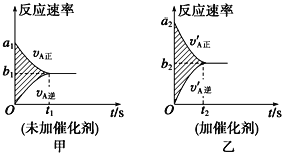
则以上所述各项正确的组合为
A. ②④⑥ B. ②④⑤ C. ②③⑤ D. ②③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年12月2日,“嫦娥三号”探测器由长征三号乙运载火箭从西昌卫星发射中心发射,首次实现月球软着陆和月面巡视勘察。“长征”系列火箭用偏二甲肼(C2H8N2)作燃料,四氧化二氮作氧化剂,生成氮气和二氧化碳气体。
(1)写出反应的化学方程式:_____________________________________________。
(2)该反应是________(填“放热”或“吸热”)反应,反应物的总能量________(填“大于”“小于”或“等于”)生成物的总能量,断开化学键________的总能量小于形成化学键________的总能量(填“吸收”或“放出”)。
(3)如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的,这个规律称为盖斯定律。据此回答下列问题。
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。丙烷脱氢可得丙烯。
已知:C3H8(g)―→CH4(g)+HC≡CH(g)+H2(g) ΔH1=+156.6 kJ·mol-1
CH3CH=CH2(g)―→CH4(g)+HC≡CH(g) ΔH2=+32.4 kJ·mol-1
则相同条件下,丙烷脱氢得丙烯的热化学方程式为________________________________。
(2)已知:Na2CO3·10H2O(s)===Na2CO3(s)+10H2O(g)ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2OH++OH-△H>0,下列叙述正确的是( )
A.向平衡体系中加入水,平衡正向移动,c (H+)增大
B.将水加热,Kw增大,pH不变
C.向水中加入少量硫酸氢钠固体, ![]() 增大
增大
D.向水中加入少量NaOH固体,平衡正向移动,c(H+)降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质之间的相互关系错误的是
A. 干冰和冰是同一种物质
B. CH3CH20H和CH3 0CH3互为同分异构体
C. 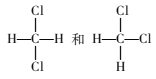 是同一种物质
是同一种物质
D. 金刚石和石墨互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z、R原子序数依次增大。考古时利用W的一种同位素测定一些文物的年代,X是地壳中含量最多的元素,Y、Z的质子数分别是W、X的质子数的2倍。下列说法错误的是
A. Y单质可以与WX2发生置换反应
B. 工业上常用电解熔融的Y与R形成的化合物的方法制取Y
C. 原子半径:Y>Z>R;简单离子半径:Z>X>Y
D. 可以用澄清的石灰水鉴别WX2与ZX2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学可以为人类制备新物质,还可以提供能源。
(1)乳酸能与金属铁反应制备一种药物,配平下列化学方程式:____。
![]()
这个反应中的还原产物的化学式是____
(2)已知氢气完全燃烧生成1 mol的液态水放出286 kJ热量,某宇宙飞船上使用的氢氧燃料电池每产生1 kw![]() h电能生成570 g液态水,该电池能量转化率为____
h电能生成570 g液态水,该电池能量转化率为____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列常见物质的俗名与化学式对应正确的是
A. 纯碱——NaOH B. 生石灰——Ca(OH)2
C. 胆矾——CuS04 D. 石英——SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
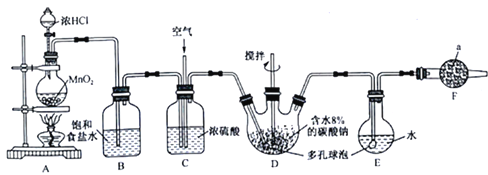
【题目】Cl2O为国际公认的高效安全灭菌消毒剂之一,实验室可利用氧气和空气(氯气与空气体积比为1∶3,空气不参与反应)的混合气与含水8%的碳酸钠反应制备,所用实验装置和Cl2O的性质如下:
颜色 | 棕黄色 |
状态 | 气体 |
气味 | 强刺激性 |
熔点 | -116℃ |
沸点 | 3.8℃ |
水溶性 | 极易溶于水,与水反应生成次氯酸 |
热稳定性 | 42℃以上,分解为Cl2和O2 |
回答下列问题:
(1)仪器a的名称为_______________,所盛放的药品是_____________________。
(2)写出装置A 中发生的离子方程式:_____________________________。
(3)装置C的主要作用是_______________________________________。
(4)装置D、E 中都用到多孔球泡,其作用是____________________________。
(5)写出装置D生成Cl2O的化学方程式:___________________________。
(6)Cl2O是一种更为理想的饮用水消毒剂,ClO2和Cl2O在消毒时自身均被还原为Cl-,ClO2的消毒能力是等质量Cl2O的______________ (结果保留两位小数)倍。
(7)装置E中所得溶液呈黄绿色,可能的原因是D中的氯气过量进入E中,设计实验证明:____________________________________________________________。
(8)制备Cl2O装置中存在缺陷,请提出改进措施:_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com