
【题目】一定物质的量的Cl2与NaOH溶液反应,所得产物中含NaClO和NaClO3物质的量之比为3∶5,则参加反应的Cl2与NaOH物质的量之比为( )
A. 8∶11 B. 3∶5 C. 1∶2 D. 18∶8
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色) ![]() 2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )
2CrO42-(黄色)+2H+ 。用K2Cr2O7溶液进行下列实验,结合实验,下列说法不正确的是( )
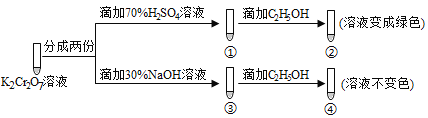
A. ①中溶液橙色加深,③中溶液变黄 B. ②中Cr2O72-被C2H5OH还原
C. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色 D. 对比②和④可知K2Cr2O7酸性溶液氧化性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产硫酸的主要反应:2SO2(g)+O2(g)![]() 2SO3(g)△H<0。图中L(L1、L2)、X可分别代表压强或温度。下列说法正确的是
2SO3(g)△H<0。图中L(L1、L2)、X可分别代表压强或温度。下列说法正确的是
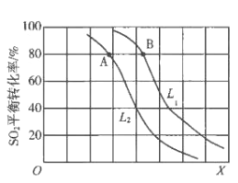
A. X代表压强
B. 推断L1>L2
C. A、B两点对应的平衡常数相同
D. 一定温度下,当混合气中n(SO2):n(O2):n(SO3)=2:1:2,则反应一定达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 1 mol H2O的质量为18g/mol
B. CH4的摩尔质量为16g
C. 3.01×1023个SO2分子的质量为32g
D. 标准状况下,1 mol任何物质体积均为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积为1L干燥容器中充入HCl气体后,测得容器中气体对氧气的相对密度为1.082。将此气体倒扣在水中,进入容器中液体的体积是
A. 0.25L B. 0.5L C. 0.75L D. 1L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组模拟氯碱工业生产原理并探究其产品的性质。已知文献记载:
①氯气与冷的氢氧化钠溶液反应生成NaClO;氯气与热的氢氧化钠溶液反应可生成NaClO和NaClO3。②在酸性较弱时KI只能被NaClO氧化,在酸性较强时亦能被NaClO3氧化。
(1)该小组利用如图所示装置制取家用消毒液(主要成分为NaClO),则a为_______(填“阳极”或“阴极”)。生成NaClO的离子方程式为________。
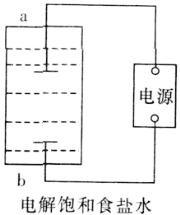
(2)该小组将0.784L(标准状况)Cl2通入50.00mL热的NaOH溶液中,两者恰好完全反应后,稀释到250.0mL。
Ⅰ.取稀释后的溶液25.00mL用醋酸酸化,加入过量KI溶液。用0.2000mol·L-1 Na2S2O3溶液滴定:I2+2S2O32-=2I-+S4O62-,消耗Na2S2O3溶液10.00mL时恰好到达终点。
Ⅱ.将上述滴定后的溶液用盐酸酸化至强酸性,再用上述Na2S2O3溶液滴定到终点,需Na2S2O3溶液30.00mL。
①操作Ⅱ中氯酸钠与碘化钾反应的离子方程式为________。
②反应后的溶液中次氯酸钠和氯酸钠的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子核外电子是分层排布的,下列关于L层与M层的说法不正确的是( )
A.L层离核比M层离核近
B.电子在M层上运动时所具有的能量高于L层
C.当L层上的电子数为奇数时,M层上不可能有电子
D.当L层上的电子数为偶数时,M层上一定有电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
① | ||||||||
② | ③ | |||||||
④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)④在周期表中的位置是______,③的最简单氢化物的电子式______。
(2)②、⑥、⑧对应的最高价含氧酸的酸性由强到弱的顺序是______(填化学式)。
(3)①、②、③三种元素形成的化合物M中原子个数比为4∶2∶3,M中含有的化学键类型有______。
(4)能说明⑦的非金属性比⑧的非金属性______(填“强”或“弱”)的事实是______(用一个化学方程式表示)。
(5)⑤、⑧两元素最高价氧化物对应水化物相互反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题。(除特别注明外,其他一律用化学式表示)

(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为____________。
(2)元素E的最高价氧化物的电子式是________________。
(3)某元素二价阳离子的核外有10个电子,该元素是____________(填元素名称)。
(4)G、H、I形成的气态氢化物稳定性由强到弱的顺序: _________________。
(5)H、J、K的最高价氧化物的水化物的酸性由强到弱的顺序: ______________。
(6)元素B的最高氧化物的水化物的电子式是______________,化合物类型为________________(填“离子化合物”或“共价化合物”)。
(7)元素I的氢化物的结构式为____________;该氢化物常温下和元素K的单质反应的化学方程式为_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com