
【题目】Na与Na+两种粒子中,相同的是
A.化学性质B.质子数C.最外层电子数D.核外电子层数
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是短周期元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。
(1) HWO的结构式为____。
(2) ①X、Y、Z、W原子半径由大到小依次是____(填元素符号)。
②X、Z、W最高价氧化物水化物酸性由强到弱依次是_________。(填化学式)。
(3) W同族上一周期元素单质不能把W元素从其钠盐的水溶液中置换出来,用化学方程式解释____________________。
(4) ①家用“管道通”的有效成分是烧碱和Y的单质,使用时需加入一定量的水,此时发生反应的化学方程式为_________________________。
②含Y元素的盐与小苏打溶液可用作泡沫灭火剂,写出灭火时发生反应的离子方程式__________________________________。
(5) NW3是黄色油状液体,无漂白性,在热水中会发生水解。NW3的电子式为____。若取该液体滴入50℃左右的热水中,片刻后取该热水溶液滴到干燥的红色石蕊试纸上,试纸先变蓝后褪色。写出NW3在热水中发生水解的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得出相应结论的是
方法 | 现象 | 结论 | |
A | 观察氯水颜色 | 氯水呈黄绿色 | 氯水中含Cl2 |
B | 向饱和NaHCO3溶液中加入足量氯水 | 有无色气体产生 | 氯水中含HClO |
C | 向红色纸条上滴加氯水 | 红色纸条褪色 | 氯水具有漂白性 |
D | 向FeCl2溶液中滴加氯水 | 溶液变成棕黄色 | 氯水具有氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种有机化合物甲、乙的球棍模型如图所示,下列说法错误的是
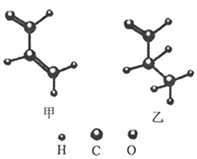
A. 甲、乙互为同系物,都能使酸性高锰酸钾溶液褪色
B. 甲分子中所有原子可能处于同一平面内
C. 用红外光谱能区分甲、乙两种物质
D. 一定条件下,甲与足量H2反应后,可得到1-丙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物HOCH2![]() COOH是一种重要的化工原料,下列有关该有机物的说法正确的是
COOH是一种重要的化工原料,下列有关该有机物的说法正确的是
A. 分子中最多有6个碳原子共面
B. 能发生加成、氧化、取代、消去反应
C. 在一定条件下,能生成环状酯
D. 1mol该有机物与足量金属钠反应最多能生成0.5mo1H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使用容量瓶配制溶液时,由于操作不当会引起误差,下列情况会使所配溶液偏高的是
A. 定容时,俯视容量瓶的刻度线
B. 转移溶液前容量瓶内有少量蒸馏水
C. 溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
D. 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
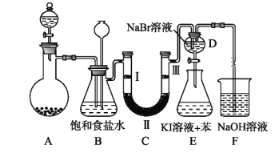
(1) 制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:_____________。
装置B中饱和食盐水的作用是___________________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象____________________________________。
(2) 装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入__________。
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3) 设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,离子反应方程为:_______________________,打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是__________________________________。
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的离子方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.2 g铜粉与一定量的浓硝酸反应,当铜粉完全反应时收集到气体1.12 L(标准状况下)。则所消耗硝酸的物质的量是( )
A. 0.55mol B. 0.15 mol C. 0.3 mol D. 0.11mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com