
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
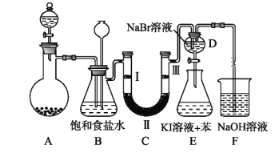
(1) 制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:_____________。
装置B中饱和食盐水的作用是___________________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象____________________________________。
(2) 装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入__________。
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3) 设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,离子反应方程为:_______________________,打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是__________________________________。
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的离子方程式:_____________。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 除去Cl2中的HCl B中长颈漏斗中液面上升,形成水柱 d Cl2+2Br-= Br2+2Cl- E中溶液分为两层,上层(苯层)为紫红色 2OH-+Cl2
MnCl2+Cl2↑+2H2O 除去Cl2中的HCl B中长颈漏斗中液面上升,形成水柱 d Cl2+2Br-= Br2+2Cl- E中溶液分为两层,上层(苯层)为紫红色 2OH-+Cl2![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
【解析】
(1)二氧化锰与浓盐酸反应生成氯化锰、氯气和水;制取的氯气中含有氯化氢杂质,依据氯气和氯化氢气体的性质选择合适的除杂剂,结合装置中气体压强变化分析现象;
(2)验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性;
(3)氯气的氧化性强于溴,溴的氧化性强于碘,结合萃取现象解答;
(4)氯气有毒,直接排放容易造成空气污染,氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,可以被氢氧化钠吸收。
(1)二氧化锰与浓盐酸反应生成氯化锰、氯气和水,方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;制取的氯气中含有氯化氢杂质,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,选择饱和食盐水吸收氯气中的氯化氢,装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,发生堵塞时B中的,压强增大,B中长颈漏斗中液面上升,形成水柱;
MnCl2+Cl2↑+2H2O;制取的氯气中含有氯化氢杂质,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,选择饱和食盐水吸收氯气中的氯化氢,装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,发生堵塞时B中的,压强增大,B中长颈漏斗中液面上升,形成水柱;
故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;除去Cl2中混有的HCl;B中长颈漏斗中有水柱上升;
MnCl2+Cl2↑+2H2O;除去Cl2中混有的HCl;B中长颈漏斗中有水柱上升;
(2)装置C的实验目的是验证氯气是否具有漂白性,验证氯气是否具有漂白性,要验证干燥氯气无漂白性,湿润的有色布条中,氯气和水反应生成次氯酸具有漂白性,选项中abc的Ⅱ中都是干燥剂,再通入湿润的有色布条不能验证氯气的漂白性,所以C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,所以选d;
故答案为:d;
(3)D中是溴化钠,当向D中缓缓通入少量氯气时,氯气和溴化钠反应生成溴单质,其离子方程式为:Cl2+2Br-= Br2+2Cl-;溴单质的氧化性强于碘单质,溴单质和碘化钾反应生成碘单质,碘单质溶于苯呈紫红色,振荡.观察到的现象是:E中溶液分为两层,上层(苯层)为紫红色;
故答案为:Cl2+2Br-= Br2+2Cl-;E中溶液分为两层,上层(苯层)显紫红色;
(4)氯气有毒,直接排放容易造成空气污染,氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,可以被氢氧化钠吸收,反应的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。

下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列方法制取氢气,反应速率最大的是
A.冬天,块状锌与2 mol·L一1硫酸溶液反应
B.冬天,粉末状锌与2 mol·L一1硫酸溶液反应
C.夏天,块状锌与2 mol·L一1硫酸溶液反应
D.夏天,粉末状锌与2mol·L一1硫酸溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容密闭容器中,不能说明反应NH2COONH4(s)![]() 2NH3(g)+CO2(g)达到平衡状态的是
2NH3(g)+CO2(g)达到平衡状态的是
A. 混合气体的平均相对分子质量不再发生变化
B. 混合气体的密度不再发生变化
C. 混合气体的总物质的量不再发生变化
D. 混合气体的压强不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效、安全的消毒剂。实验室以NH4Cl、盐酸和NaClO2(亚氯酸钠)为原料制备ClO2的流程如图所示。

请回答下列问题:
(1)ClO2中Cl的化合价是________________________。
(2)写出电解时发生反应的化学方程式:____________________________。
(3)NCl3与NaClO2(亚氯酸钠)反应的化学方程式NCl3+3H2O+6NaC1O2=6ClO2↑+3NaCl+3NaOH+NH3↑,该反应的氧化剂与还原剂的物质的量之比为______;若产生11.2L(标准状况)NH3,则转移电子的总数为___NA。
(4)二氧化氯进行水处理时,除了杀菌消毒外,还能除去水中的Fe3+和Mn2+,写出C1O2将Mn2+氧化为MnO2的离子方程式(C1O2反应后的产物为Cl-):_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写及评价均合理的是( )
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应: Ba2++HCO3-+OH-===BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
D | 1 mol/L的NaAlO2溶液和2.5 mol/L的HCl溶液等体积混合: 2AlO2-+5H+===Al3++Al(OH)3↓+H2O | 正确;第一步反应和第二步反应消耗的H+的物质的量之比为2∶3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。下列说法正确的是
A. 7.8 g Na2O2中含有的阴离子数为0.2NA。
B. 1 mol Fe溶于过量硝酸,电子转移数为2NA
C. 22.4 L(标准状况下)氩气含有的质子数为18NA
D. 标准状况下,2.24 L N2和O2的混合气体中分子数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com