
| A. | 石油干馏可得到汽油、煤油等 | |
| B. | 苯不能使酸性KmnO4溶液褪色,因此苯不能发生氧化反应 | |
| C. | 淀粉、蛋白质完全水解的产物互为同分异构体 | |
| D. | 乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
分析 A.石油分馏产品得到汽油、煤油等,煤的干馏产物含煤焦油等;
B.苯与高锰酸钾不反应,但苯可燃烧;
C.淀粉水解产物最终为葡萄糖,而蛋白质的水解最终产物为氨基酸;
D.乙酸乙酯、油脂均含-COOC-.
解答 解:A.石油分馏产品得到汽油、煤油等,煤的干馏产物含煤焦油等,不存在石油干馏,故A错误;
B.苯与高锰酸钾不反应,但苯可燃烧,燃烧反应属于氧化反应,故B错误;
C.淀粉水解产物最终为葡萄糖,而蛋白质的水解最终产物为氨基酸,葡萄糖与氨基酸的组成不同,不是同分异构体,故B错误;
D.乙酸乙酯、油脂均含-COOC-,在NaOH溶液发生水解反应,分别售出乙醇、甘油,均有醇生成,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的性质、有机反应、同分异构体判断为解答的关键,侧重分析与应用能力的考查,注意化石能源的综合应用,题目难度不大.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:计算题
 实验室测定常温下l molH2的体积通常用如图所示的装置.
实验室测定常温下l molH2的体积通常用如图所示的装置.| 实验次数 | 镁带质量(g) | 硫酸体积( mL) | 氢气体积( mL) | l摩尔气体的体积(L)(精确到0.001L) |
| 1 | 0.050 | 10 | 49.0 | |
| 2 | 0.049 | 10 | 48.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X、Y与Z的原子半径大小:Y>Z>X | |
| B. | 元素W、Z的氯化物中,化学键类型相同,且各原子均满足8电子 | |
| C. | 元素X与元素Y形成的化合物是一种较好的耐火材料 | |
| D. | 元素X可与元素Z可组成3种二价阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
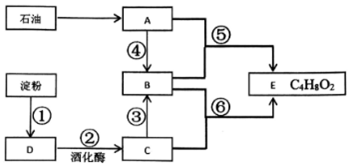
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用分液的方法可以分离汽油和水 | |
| B. | 酒精灯加热试管时须垫石棉网 | |
| C. | NH3能使湿润的蓝色石蕊试纸变红 | |
| D. | 盛放NaOH溶液的广口瓶,可用玻璃塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
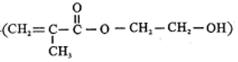 )可由下列方法合成:
)可由下列方法合成: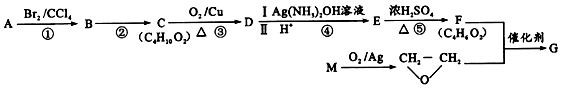
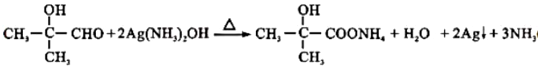 .B→C反应方程式为
.B→C反应方程式为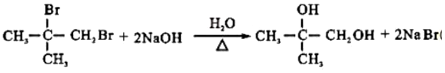 .
.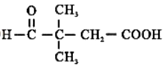 ,
, .
.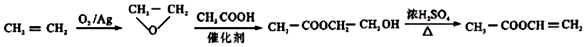 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用图表示. 下列关于海洋氮循环的说法正确的是( )
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用图表示. 下列关于海洋氮循环的说法正确的是( )| A. | 海洋中的氮循环起始于氮的氧化 | |
| B. | 海洋中的氮循环属于固氮作用的是③ | |
| C. | 海洋中的反硝化作用一定有氧气的参与 | |
| D. | 向海洋排放含NO3-的废水会影响海洋中NH4+的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
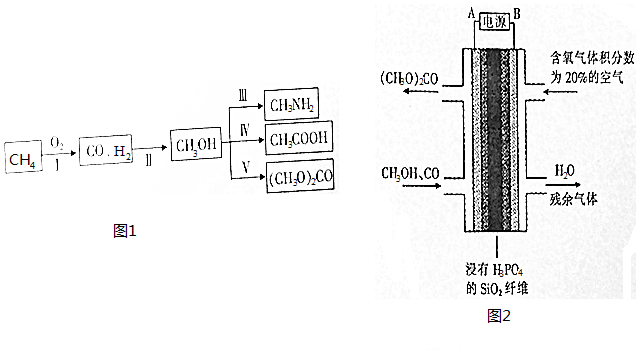
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若C溶于水后得到强碱溶液,则A可能是Na | |
| B. | 若向C溶液中逐滴加入NaOH溶液,溶液中出现白色沉淀并逐渐消失,则A可能Al | |
| C. | 若C的溶液遇NaHCO3固体,放出CO2气体,则A可能是H2 | |
| D. | 若C的溶液中滴加NaOH产生白色沉淀,后白色沉淀消失,则B可能为Mg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com