
 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用图表示. 下列关于海洋氮循环的说法正确的是( )
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用图表示. 下列关于海洋氮循环的说法正确的是( )| A. | 海洋中的氮循环起始于氮的氧化 | |
| B. | 海洋中的氮循环属于固氮作用的是③ | |
| C. | 海洋中的反硝化作用一定有氧气的参与 | |
| D. | 向海洋排放含NO3-的废水会影响海洋中NH4+的含量 |
分析 A.转化关系图可知海洋中的氮循环起始于氮的还原;
B.海洋中不存在游离态的氮,氮元素是以化合态存在;
C.反硝化作用是指将硝酸盐转变成氮气的过程.硝化作用是指氨在微生物作用下氧化为硝酸的过程.硝化细菌将氨氧化为硝酸的过程.反硝化作用:反硝化细菌在缺氧条件下,还原硝酸盐,释放出分子态氮(N2)或一氧化二氮(N2O)的过程;
D.转化关系图中硝酸根离子增多,反硝化作用增强;
解答 解:A.转化关系图可知海洋中的氮循环起始于氮的还原,大气氮生成铵根离子,故A错误;
B.海洋中不存在游离态的氮,氮元素是以化合态存在,主要是硝酸根离子,故B错误;
C.反硝化作用是指将硝酸盐转变成氮气的过程.硝化作用是指氨在微生物作用下氧化为硝酸的过程.硝化细菌将氨氧化为硝酸的过程.反硝化作用:反硝化细菌在缺氧条件下,还原硝酸盐,释放出分子态氮(N2)或一氧化二氮(N2O)的过程,不一定有氧参加,故C错误;
D.转化关系图中硝酸根离子增多,反硝化作用增强,向海洋排放含NO3-的废水会影响海洋中NH4+的含量,故D正确;
故选D;
点评 本题考查了含氮元素的物质的综合应用,主要是氮的循环分析,注意转化图中的信息应用,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液与过量的澄清石灰水反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| B. | 用食醋除去热水瓶水垢中CaCO3:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 向氢氧化钡溶液中滴加足量稀硫酸:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| D. | 金属钠和水反应:Na+2H2O═Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油干馏可得到汽油、煤油等 | |
| B. | 苯不能使酸性KmnO4溶液褪色,因此苯不能发生氧化反应 | |
| C. | 淀粉、蛋白质完全水解的产物互为同分异构体 | |
| D. | 乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃、l0IKPa下,NA个C18O2分子的质量为48g | |
| B. | 标准状况下,22.4L HF中含有的电子数为10NA | |
| C. | 1mol白磷(P4)分子中所含化学键的数目为4NA | |
| D. | 1L0.1 mol/L的NaClO水溶液中含有的氧原子数为0.l NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化和液化是物理变化 | |
| B. | 煤的干馏是在隔绝空气条件下进行的 | |
| C. | 大量燃烧煤炭是造成雾霾的重要原因 | |
| D. | 发展“煤制油”工程可减少对石油产品的依赖 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
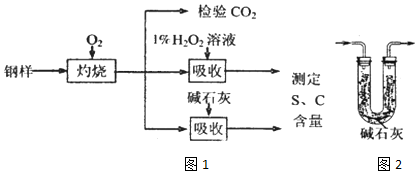
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=a的Na2A溶液中,由水电离产生的c(OH-)=10a-14 | |
| B. | 将pH=a的H2A稀释为pH=a+l的过程中,c(H2A)/c(H+)减小,则H2A为弱酸 | |
| C. | 测NaHA溶液的pH,若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 | |
| D. | 0.2 mol•L-1 H2A 溶液中的 c(H+)=a,0.1 mol•L-1 H2A溶液中的 c(H+)=b,若a<2 b,则H2A为弱酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com