
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,其最外层电子数之和等于24,由此可知说法错误的是( )
| W | X | |
| | Y | Z |
B
解析试题分析:A.W、X是同一周期的元素,原子序数越大,原子半径就越小。因此原子半径:W >X。正确。B.假设W的原子最外层电子数为a,则X为(a+1);Y为(a+1)=;Z为(a+2). 由于这四种元素原子的最外层电子数之和等于24。所以a=5.因此W是N;X是O;Y是S;Z是Cl.N的最高化合价为+5价;Cl的最高化合价为+7价,因此元素最高正价:Z >W。错误。C.同一周期的元素,从左到右,元素的非金属性逐渐增强。元素的非金属性越强,其简单离子的还原性就越弱。故简单阴离子的还原性:S2->Cl-.正确。D.X、Y是同一主族的元素,从上到下,元素的非金属性逐渐减弱。元素的非金属性越强,其氢化物的稳定性就越强。因此气态氢化物的稳定性H2O>H2S。正确。
考点:考查元素周期表、元素周期律的应用的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
某元素的最高正价与其负价的绝对值之差为4,该元素的离子与跟其核外电子排布相
同的离子形成的化合物是( )
A K2S B MgO C MgS D NaF
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中正确的是
A.所有主族元素正化合价数,等于它的族序数
B.ⅦA族元素的原子随核电荷数的增加,得电子能力逐渐减弱
C.前三周期元素中共有非金属元素12种
D.ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列排列顺序正确的是
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>F
③酸性:H3PO4>H2SO4>HClO4
④失电子能力:Na>Mg>Al
⑤晶体的熔点:SiO2>NaCl>CCl4>SO2
| A.②④⑤ | B.①②④ | C.②③⑤ | D.全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z的原子序数依次增大,Y为ⅠA族元素,X与Z同主族,3种元素原子的最外层电子数之和为13,下列判断正确的是( )
| A.Y元素位于第2周期 | B.Y、Z均能与X形成不只一种化合物 |
| C.X是VA族元素 | D.氢化物的稳定性:HnZ > HnX |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列排列顺序正确的是
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>F
③酸性:H3PO4>H2SO4>HClO4
④结合质子能力:OH->CH3COO->Cl-
⑤晶体的熔点:SiO2>NaCl>CCl4>SO2
| A.②④⑤ | B.①②④ | C.③⑤ | D.全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据表中提供的部分短周期元素原子半径及主要化合价的信息,判断以下叙述中正确的是:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
北京时间2012年9月14日,国外媒体报道,美国宇航局的“好奇”号火星车已经展开它的X射线分析器,并首次完成对火星物质元素成分的分析。下面这张图显示的是α粒子与X射线分光仪从某仪器获得的元素分析数据。多个峰值表明各种成分非常丰富,其中包括在火星大气里发现的氩,该仪器自身的铝,以及火星土壤微粒所含的硫黄和氯.
理解此图,判断下列说法错误的是
| A.峰值最高的过渡元素在周期表中的位置是第四周期第Ⅷ副族 |
B.上述元素分析图中,同一周期的两种主族元素可形成1∶1型离子化合物只有一种,其电子式为 |
| C.氯比硫的非金属性强的依据之一是HCl比H2S稳定 |
| D.工业上常用电解氧化铝的方法制备铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
是部分短周期元素化合价与原子序数的关系图,下列说法正确的是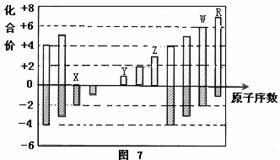
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R>W |
| C.WX和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物相互不能反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com