
【题目】某废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),设计了如下流程图:

可供选择的试剂:①饱和Na2CO3溶液;②饱和K2CO3溶液;③KOH溶液;④BaCl2溶液;⑤Ba(NO3)2溶液;⑥H2O2溶液;⑦KMnO4溶液(H+);⑧稀盐酸。
请根据流程图,回答相关问题:
(1)试剂a应该选用______(填试剂编号),反应的离子方程式为____________。
(2)萃取操作中,可以选的试剂还可以是_________。
A. 裂化汽油 B.乙醇 C.苯 D.直馏汽油
(3)除去无色液体Ⅰ中的Ca2+、Mg2+、SO42-,选出试剂b(试剂b代表一组试剂)所代表的试剂,按滴加顺序依次是__________。(填试剂序号)
(4)调节pH的作用是___________________________________。
(5)操作①的名称是_____,操作②中用到的硅酸盐仪器除酒精灯、玻璃棒外还有________。
【答案】 ⑥ H2O2+2Br—+2H+=Br2+2H2O CD ④③②(或④②③或③④②) 除去过量的CO32—、OH— 蒸馏 蒸发皿
【解析】本题考查化学工艺流程,(1)根据流程以及废液中所含离子,加入CCl4溶液出现橙色液体,说明试剂a的作用把Br-氧化成Br2,试剂a应为氧化剂,且不能引入新杂质,即试剂a为H2O2,反应的离子方程式为2Br-+H2O2+2H+=Br2+2H2O;(2)选择萃取剂原则是①所选萃取剂不能与原溶剂互溶;②被萃取物质不能与萃取剂反应;③被萃取剂物质在萃取剂的溶解度要大于在原溶剂中的溶解度,A、裂化汽油中含有碳碳不饱和键与溴水发生加成反应,不能作萃取剂,故A错误;B、乙醇溶于水,本实验中不能作萃取剂,故B错误;C、苯不溶于水,且不与溴水反应,溴易溶于有机溶剂中,因此可以作萃取剂,故C正确;D、直馏汽油不溶于水,且不与溴水反应,溴易溶于有机溶剂中,因此可以作萃取剂,故D正确;(3)本题中Ca2+用K2CO3除去,Mg2+用KOH除去,SO42-用Ba2+除去,K2CO3不仅除去Ca2+,还要除去过量的Ba2+,因此K2CO3放在Ba2+的后面,即所加试剂的顺序是④③②或④②③或③④②;(4)无色溶液II中含有CO32-和OH-,因此调节pH的目的是除去过量的CO32-和OH-;(5)Br2易溶于CCl4,因此操作①是蒸馏;操作②是蒸发结晶,还需要用到的硅酸盐仪器是蒸发皿。


科目:高中化学 来源: 题型:
【题目】已知:p(Ba2+)=-lgc(Ba2+), p(酸根离子)=-lgc(酸根离子),酸根离子为SO42-或CO32-。某温度下BaSO4、BaCO3的沉淀溶解关系如图所示,下列叙述正确的是
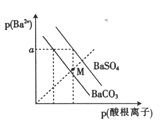
A. p(Ba2+)=a时,溶液中c(SO42-)>c(CO32-)
B. M点对应的溶液中有BaCO3 沉淀生成
C. 由图可知该温度下:Ksp(BaSO4)3)
D. BaSO4 沉淀不能转化为BaCO3 沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉水解产物,某学生设计了如下实验方案:

回答下列问题:
(1)试剂1是_____________;
(2)试剂2是_____________,作用是_______________________;
(3)如何检验第①步实验已基本完成_________________________________________。
(4)写出淀粉酿酒过程涉及到化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中既属于化合反应,又属于氧化还原反应的是( )
A. SO2+H2O2=H2SO4B. Zn+2AgNO3=Zn(NO3) 2+2Ag
C. 2HClO=2HCl+O2↑D. CO2+2NaOH=Na2CO3+H2 O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核安全与放射性污染防治已引起世界核大国的广泛重视。在爆炸的核电站周围含有放射性物质碘一131和铯一 137。碘—131—旦被人体吸入,可能会引发甲状腺等疾病。
(l)Cs(铯)的价电子的电子排布式为6s1,与铯同主族的前四周期(包括第四周期)的三种元素X、Y、Z的电离能如下表:
元素代号 | X | Y | Z |
第一电离能(kJ·mol-1) | 520 | 496 | 419 |
上述三种元素X、Y、Z的元素符号分别为_________,基态Z原子的核外电子排布式为______,X形成的单质晶体中含有的化学键类型是_________________。
(2)F与I同主族,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别为______、______,BeF2分子的立体构型是____________,H2O分子的立体构型是________________。
(3)与碘同主族的氯具有很强的活泼性,能形成大量的含氯化合物。BC13分子中B—C1键的键角为__________________。
(4)131I2晶体的晶胞结构如图甲所示,该晶胞中含有____个131I2分子;KI的晶胞结构如图乙所示,每个K+紧邻______个I-。

(5)KI晶体的密度为ρg cm 3,K和I的摩尔质量分别为MK g mol-1和M1g mol-1,原子半径分别为rKpm和r1 pm,阿伏加德罗常数值为NA,则KI晶胞中原子的体积占晶胞体积的百分率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A. 乙醛与银氨溶液反应:CH3CHO+2[Ag(NH3)2]++2OH-![]() CH3COO-+NH4++2Ag↓+3NH3+H2O
CH3COO-+NH4++2Ag↓+3NH3+H2O
B. 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O
C. 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
D. 溴乙烷水解生成乙醇:CH3CH2Br+OH-![]() CH3CH2OH+Br-
CH3CH2OH+Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用20g氢氧化钠固体配成1 mol·L﹣1的NaOH溶液,所得溶液的体积是
A.1000 mL B. 500 mL C.100 mL D.50 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯是工业上常用的化工原料,可以用于合成安息香酸苄酯和高分化合物G (部分反应条件略去),流程如下所示,请回答下列问题:
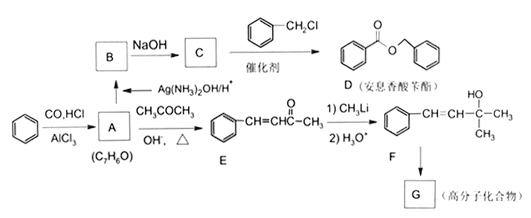
(1)C的化学名称是____________,B中的官能团名称是____________。
(2)E分子中最多有____________个原子共平面;G的结构简式为____________;
(3)C生成D的反应类型为____________。
(4)A生成E的化学方程式为_____________________________________。
(5)H是D的同分异构体,分子中含有酯基,有两个苯环且不直接相连,符合上述条件的结构有____________种,其中核磁共振氢谱图有6组峰,且面积比为3∶2∶2∶2∶2∶1的同分异构体的结构简式为____________(写出一种即可)。
(6)参照上述合成路线,以2-氯丙烷为原料,其它无机试剂和有机溶剂任选,设计2-甲基-2-丙醇的合成路线____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA 表示阿伏加德罗常数,下列说法正确的是
A. T ℃时,1 L pH=6纯水中,含10-8NA个![]()
B. 15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.4NA
C. 1 mol SiO2中含有2 mol Si–O单键
D. 14g分子式为CnH2n的(n≥2)链烃中含有的C=C的数目一定为NA/n
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com