
科目:高中化学 来源: 题型:
| A、除去乙烷中的乙烯:在光照条件下通入Cl2,气液分离 |
| B、除去乙醇中的乙酸:加足量生石灰后蒸馏 |
| C、“硝基苯制备”实验中,浓硫酸起氧化作用 |
| D、用溴水不能验证裂化汽油中含有不饱和烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2S既是氧化产物,又是还原产物 |
| B、产物中的SO42-部分有一部分是氧化产物 |
| C、5mol FeS2发生反应时,有10mol电子转移 |
| D、FeS2只做还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | Li | C | N | O | F | Ne | ||
| 三 | Na | Mg | S | Cl | ||||
| 四 | K | Ca | Br |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
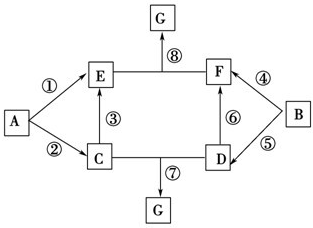 A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).
A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度时,在2L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:
某温度时,在2L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com