
【题目】某工厂排放的工业废水中含Fe3+、Al3+、Cu2+ , 为了减少环境污染,变废为宝,利用废铁屑制得Fe2O3、Al2O3和金属Cu,过程如下.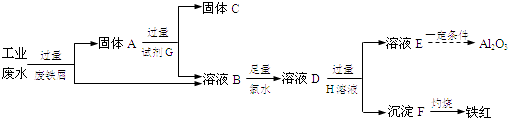
请回答:
(1)固体A的成分是(填化学式).
(2)溶液B中的金属阳离子有 .
(3)B→D反应的离子方程式是 .
(4)试剂G是(填名称).
【答案】
(1)Fe和Cu
(2)Fe3+、Al3+、Fe2+
(3)2Fe2++Cl2=2Fe3++2Cl﹣
(4)盐酸
【解析】解:由流程可知,某工厂排放的工业废水中含Fe3+、Al3+、Cu2+ , 先加过量铁2Fe3++Fe═3Fe2+ , 铁在金属活动顺序表中排在铜的前面,所以铁粉把铜置换出来,发生Fe+Cu2+═Cu+2Fe2+ , 由于铁过量,可知固体A中含Fe和Cu;试剂G为盐酸,Cu与盐酸不反应,则固体C为Cu,溶液B中含Fe3+、Al3+、Fe2+ , 加氯水,+2价的铁离子被氯水氧化,2Fe2++Cl2=2Fe3++2Cl﹣;再加过量D为NaOH,溶液E为偏铝酸钠,沉淀F为Fe(OH)3 , (1)由上述分析可知,A为Fe和Cu,所以答案是:Fe和Cu;(2)溶液B中的金属阳离子有Fe3+、Al3+、Fe2+ , 所以答案是:Fe3+、Al3+、Fe2+;(3)B→D反应的离子方程式是2Fe2++Cl2=2Fe3++2Cl﹣ , 所以答案是:2Fe2++Cl2=2Fe3++2Cl﹣;(4)由上述分析可知,G为盐酸,所以答案是:盐酸.


科目:高中化学 来源: 题型:
【题目】关于图中各装置的叙述不正确的是( ) 
A.装置①是中和滴定法测定硫酸的物质的量浓度
B.装置②中手捂烧瓶(橡胶管已被弹簧夹夹紧),发现导管中有液柱上升并保持稳定,则说明装置不漏气
C.装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸
D.装置④可检验溴乙烷发生消去反应得到的气体中含有乙烯(假定每个装置中吸收完全)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各选项中的两个反应,可用同一个离子方程式表示的是( )
选项 | Ⅰ | Ⅱ |
A | Ba(OH)2溶液与过量NaHCO3溶液混合 | NaOH溶液与过量NaHCO3溶液混合 |
B | 少量SO2通入Ba(OH)2溶液中 | 过量SO2通入Ba(OH)2溶液中 |
C | BaCl2溶液与Na2SO3溶液混合 | Ba(OH)2溶液与H2SO3溶液混合 |
D | 少量NaHCO3溶液滴入澄清石灰水中 | 少量NaOH溶液滴入Ca(HCO3)2溶液中 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究硝酸的性质,某同学设计并完成如下实验:室温下,将铁片分别置于适量的浓HNO3和稀HNO3中(如图所示).
(1)气球的作用是 .
(2)A中最终溶液变为浅绿色,发生反应的离子方程式是 .
(3)B中无明显变化,该同学进一步探究如下:假设:①常温下铁与浓硝酸不反应.② . 进行实验:将B中的铁片取出并洗净后,放入CuSO4溶液中,无明显变化,则说明假设①(填“成立”或“不成立”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类的正确组合是
碱 | 酸 | 盐 | 酸性氧化物 | |
A | 纯碱 | 盐酸 | 烧碱 | 二氧化硫 |
B | 烧碱 | 硫酸 | 纯碱 | 一氧化碳 |
C | 苛性钠 | 醋酸 | 石灰石 | 水 |
D | 苛性钾 | 硝酸 | 苏打 | 三氧化硫 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学小组设计以下实验方案,测定某部分变质为碳酸钠的小苏打样品中NaHCO3的质量分数.
(1)方案一:称取一定质量样品,置于仪器a中用酒精灯加热至恒重,冷却,用托盘天平称量剩余固体质量.重复操作,计算.仪器a的名称是;其中发生反应的化学方程式为 . 实验中为保证NaHCO3分解完全需加热至恒重,判断方法是 .
(2)方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,待沉淀后,过滤,洗涤,干燥,称量固体质量,计算.
写出NaHCO3与足量Ba(OH)2溶液反应的离子方程式;实验中判断沉淀是否完全的方法是 . 过滤操作中,除烧杯、漏斗外,还要用到的玻璃仪器为 .
(3)方案三:称取一定质量样品,按如图装置进行实验: 
B装置内所盛试剂是;D装置的作用是
实验前称取17.9g样品,实验后测得C装置增重8.8g,则样品中NaHCO3的质量分数为 .
某同学认为上述测定结果(填“偏高”或“偏低”),因为实验装置还存在一个明显的缺陷是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是实验室制取少量固体氧化铜的实验,根据实验步骤,回答有关问题.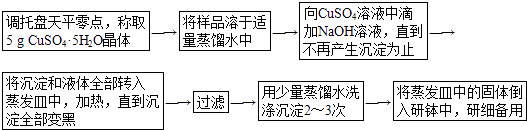
(1)调整天平零点时,若指针偏向右边,应将左边的螺丝(填“向左”或“向右”)旋动.
(2)溶解样品时要用到玻璃棒,其作用是 .
(3)反应生成沉淀的离子方程式为 .
(4)加热蒸发过程中要用到玻璃棒,其作用是 .
(5)过滤中要用到玻璃棒,其作用是 .
(6)洗涤沉淀的目的是;洗涤沉淀的方法是;为了检验沉淀是否洗涤干净,应在最后一次的洗涤液中加入溶液.
(7)若向CuSO4溶液中滴加了 100mL NaOH溶液,则NaOH溶液的物质的量浓度至少为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、1.01×105Pa时,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=+56.7kJ·mol-1自发进行的原因是( )
A.是吸热反应B.是放热反应
C.是熵减小的反应D.熵增大效应大于能量效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①干冰 ②NaHCO3晶体③氨水④纯醋酸⑤FeCl3溶液 ⑥铜 ⑦Fe(OH)3胶体 ⑧蔗糖,
(1)其中属于电解质的是 ,
(2)写出FeCl3的电离方程式: ,
(3)写出NaHCO3(aq)与稀盐酸反应的离子方程式: ,
(4)胶体是一种常见的分散系,回答下列问题.①向煮沸的蒸馏水中逐滴加入饱和FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体化学反应方程式为 .
②向Fe(OH)3胶体中加入Na2SO4饱和溶液,由于离子(填离子符号)的作用,使胶体形成了沉淀,这个过程叫做胶体的聚沉.
③区分胶体和溶液常用的方法叫做 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com