
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:实验题
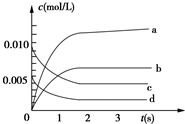 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸铝的电离方程式:Al2(SO4)3=2Al3++3SO42- | |
| B. | 小苏打的电离方程式:NaHCO3=Na++H++CO32- | |
| C. | Mg(OH)2难溶于水,所以Mg(OH)2不是电解质,而是非电解质 | |
| D. | K2CO3溶液能导电,所以K2CO3溶液是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2a=3b | |
| B. | 7b=4a | |
| C. | 原混合气体中V(H2)=bL,V(O2)=(a-b)L | |
| D. | 原混合气体中V(H2)=2(a-b)L,V(O2)=(2b-a)L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向澄清石灰水中通入足量二氧化碳:2OH?+CO2═CO32?+H2O | |
| B. | 氧化钠投入水中发生反应:O2?+H2O═2OH? | |
| C. | 醋酸溶液滴入到NaOH溶液中:CH3COOH+OH?═CH3COO?+H2O | |
| D. | 铁和稀盐酸反应制氢气:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
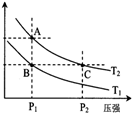 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com