
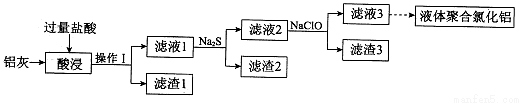
(18分)以铝灰(主要成分为Al、Al2O3,另有少量CuO、SiO2、FeO和Fe2O3杂质)为原料,可制得液体聚合氯化铝 [Alm(OH)nCl3m—n],生产的部分过程如下图所示(部分产物和操作已略去)。
(1)Al2O3与盐酸反应的离子方程式是_____________________。
(2)滤渣I是__________。滤渣2为黑色,该黑色物质的化学式是___________。
(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。其中NaClO的作用是___________。该过程发生反应的离子方程式为______________。
(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。该反应的化学方程式为_____________________。
(5)Na2S溶液呈碱性的原因是________(用离子方程式表示)。该溶液中c(Na+)=________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年四川省宜宾市高三第二次诊断测试化学试卷(解析版) 题型:选择题
25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如下图所示。下列说法正确的是

A.稀释前,c(HX)=0.01 mol/L B.稀释10倍,HX溶液的pH=3
C.a、b两点:c(X-)>c(Cl-) D.溶液的导电性:a>b
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:填空题
(12分)【化学——有机化学基础】松油醇(G)可用于配制香精,其合成路线如下:


请回答下列问题:
(1)G所含两种官能团的名称分别是________、__________。
(2)同时符合下列两个条件的B的同分异构体有____________种。
i.含有六元碳环,碳环上仅有两个取代基且呈对位;
ii.在一定条件下能发生银镜反应、水解反应和消去反应。
(3)为了鉴别E和F,宜选用下列试剂中的_______作鉴别试剂(填下列序号字母)。
a.溴水 b.银氨溶液 c.酸性KMnO4溶液 d.NaHCO3溶液
(4)C→D的化学方程式为_________________。
(5)物质A(分子式为C7H10O3)催化氢化得到H(分子式为C7H12O3),H在一定条件下可以生成高聚物I,I的结构简式为_____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三下学期3月一模化学试卷(解析版) 题型:填空题
(18分)X、Y、Z、W、E五种短周期元素在元素周期表的位置如图。其中W的原子序数是Y的2倍。

(1)能证明X、Z两元素非金属性强弱的离子方程式为
(2)一定条件下,在恒容容器中,充人一定量的WY2 (g)和XY (g),发生反应:
 时,各物质的平衡浓度如下表:
时,各物质的平衡浓度如下表:

①若温度升高到 T2℃时,反应的平衡常数为6.64,则该反应的逆反应为______反应(填“吸热”或“放热”)。
②其他条件不变,若该反应在恒压条件下进行,平衡时XY的转化率a2______a1(T1℃时的转化率)(填“<”“>”“=”)
(3)室温下,Mg(OH)2饱和溶液______(填“能”或“不能”)使石蕊试液变蓝,通过计算说明原因(已知: 。答
。答
(4)化学反应 在工业生产中有重要的地位,若要提高E2的转化率,可采取的措施是______(填字母代号)
在工业生产中有重要的地位,若要提高E2的转化率,可采取的措施是______(填字母代号)
a.升高温度 b.加催化剂 c.增加H2的浓度 d.分离出EH3
一定条件下,1mol E2与3molH2在密闭容器中反应达到平衡,E2的转化率为25%且放出23.lkJ能量,则该条件下反应的热化学反应方程式为____________________.
(5)电化学降解法可用于治理水中硝酸盐的污染,其原理如图所示。其中B为电源的______极,其电极反应式为______。

查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三下学期3月一模化学试卷(解析版) 题型:选择题
化学与生活、社会密切相关。下列说法不正确的是

A.上图是纪念发现奎宁150周年邮票,邮票中的仪器有容量瓶和研钵
B.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
C.利用可降解的生物质材料“玉米塑料”(主要成分为聚乳酸)替代一次性饭盒,可减少白色污染的产生
D.棉布、羊毛和涤纶燃烧后都只生成二氧化碳和水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东肥城市高三一模理综化学试卷(解析版) 题型:选择题
下列实验操作错误的是
A.萃取、分液前需对分液漏斗检漏
B.制取硝基苯时,采取水浴加热,将温度计插入水浴液中
C.点燃甲烷、氢气、乙烯、CO等可燃性气体前必须验纯
D.液溴保存时液面覆盖一层水,装在带橡胶塞的细口试剂瓶中
查看答案和解析>>
科目:高中化学 来源:2014-2015学年宁夏银川市高三下学期第一次模考理综化学试卷(解析版) 题型:填空题
(14分)以下是处于研究阶段的“人工固氮”的新方法.N2在催化剂表面与水发生反应:
2N2(g)+6H2O(l)4NH3(g)+3O2(g) △H=+ 1530.4kJ/mol;完成下列填空:
(1)该反应平衡常数K的表达式 .
(2)上述反应达到平衡后,保持其他条件不变,升高温度,重新达到平衡,则 .
a.平衡常数K增大
b.H2O的浓度减小
c.容器内的压强增大
d.v逆(O2)减小
(3)研究小组分别在四个容积为2升的密闭容器中,充入N2 1mol、H2O 3mol,在催化剂条件下进行反应3小时.实验数据见下表:
序号 | 第一组 | 第二组 | 第三组 | 第四组 |
t/℃ | 30 | 40 | 50 | 80 |
NH3生成量/(10﹣6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
第四组实验中以NH3表示反应的速率是 ,与前三组相比,NH3 生成量最小的原因可能是 .
(4)氨水是实验室常用的弱碱.
①往CaCl2溶液中通入CO2至饱和,无明显现象.再通入一定量的NH3后产生白色沉淀,此时溶液中一定有的溶质是 .请用电离平衡理论解释上述实验现象 .
②向盐酸中滴加氨水至过量,该过程中离子浓度大小关系可能正确的是 .
a.c(C1﹣)=c(NH4+)>c(H+)=c(OH﹣)
b.c(C1﹣)>c(NH4+)=c(OH﹣)>c(H+)
c.c(NH4+)>c(OH﹣)>c(C1﹣)>c(H+)
d.c(OH﹣)>c(NH4+)>c(H+)>c(C1﹣)
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省湖州市高三上学期期末考试化学试卷(解析版) 题型:选择题
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成甲、乙两份。向甲中逐渐加入铜粉,最多能溶解9.6g铜粉。向乙中逐渐加入铁粉,最多能溶解14.0g铁粉。 (假设硝酸只被还原为NO气体)。下列分析或结果错误的是
A.原混合酸中NO3—物质的量为0.1 mol
B.乙中最多产生气体是0.2mol
C.原混合酸中HNO3浓度为1.0 mol·L-1
D.原混合酸中H2SO4浓度为2.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015宁夏银川市高二下学期3月月考化学试卷(解析版) 题型:选择题
下列分子中既含有极性键又含有非极性键且为极性分子的是
A.CS2 B.CH4 C.CH3CH2Cl D.CH≡CH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com