
【题目】Ba(NO3)2可用于生产烟花。某主要生产BaCl2、BaCO3、BaSO4的化工厂利用某种钡泥[主要含有BaCO3、Ba(FeO2)2、极少量CuCO3等]制取Ba(NO3)2晶体,其部分工艺流程如下:

已知:Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7。
(1)酸溶时不使用浓硝酸的原因是________。
(2)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为___________。
(3)该厂结合本厂实际,中和选用的X为____________(填化学式);中和使溶液中________(填离子符号)的浓度减少(中和引起的溶液体积变化可忽略)。
(4)滤液得到Ba(NO3)2晶体的操作依次为_____________、_____________、过滤。
(5)为了减少环境污染,请对上述流程中不合理的设计进行改进,改进措施是_______。
【答案】浓HNO3易挥发、分解 Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O BaCO3 Fe3+、H+ 蒸发浓缩 冷却结晶 洗涤废渣并回收洗涤液
【解析】
BaCO3中含有Ba(FeO2)2、极少量CuCO3等,其中Ba(FeO2)2中钡元素为+2价,铁元素为+3价,加入硝酸,在容器中充分溶解得到溶液,此溶液中含有钡离子、铜离子、三价铁离子,可加入X碳酸钡,调节溶液pH=4~5,使铁离子、铜离子水解生成氢氧化铁沉淀、氢氧化铜沉淀,过滤后滤渣为氢氧化铁、氢氧化铜,滤液中主要含有硝酸、硝酸钡,经蒸发浓缩,冷却结晶,过滤得到硝酸晶体,据此分析解答。
BaCO3中含有Ba(FeO2)2、极少量CuCO3等,其中Ba(FeO2)2中钡元素为+2价,铁元素为+3价,加入硝酸,在容器中充分溶解得到溶液,此溶液中含有钡离子、铜离子、三价铁离子,可加入X碳酸钡,调节溶液pH=4~5,使铁离子、铜离子水解生成氢氧化铁沉淀、氢氧化铜沉淀,过滤后滤渣为氢氧化铁、氢氧化铜,滤液中主要含有硝酸、硝酸钡,经蒸发浓缩,冷却结晶,过滤得到硝酸晶体,
(1)浓HNO3易挥发、分解,则酸溶时不宜使用浓硝酸;
故答案为:浓HNO3易挥发、分解;
(2)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应生成硝酸钡、硝酸铁和水,反应的化学方程式为Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;
故答案为:Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;
(3)该厂结合本厂实际,中和选用的X必须能消耗过量的硝酸并使铁离子沉淀而除去,且不引入新杂质,可为BaCO3;中和使溶液中Fe3+、H+的浓度减少;
故答案为:BaCO3;Fe3+、H+;
(4)滤液中主要含有硝酸、硝酸钡,则滤液得到Ba(NO3)2晶体的操作依次为蒸发浓缩,冷却结晶,过滤;
故答案为:蒸发浓缩;冷却结晶;
(5)为了减少环境污染,请对上述流程中不合理的设计进行改进,改进措施是洗涤废渣并回收洗涤液;
故答案为:洗涤废渣并回收洗涤液。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】丙三酸是一种有机酸,用H3A表示。25℃时,向1molL-1的H3A溶波中逐滴加入NaOH溶液,滴加过程中各种含A微粒物质的物质的量分数(δ)随溶液pH的变化曲线如图所示。下列相关说法错误的是( )
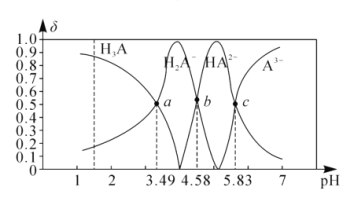
A.a点溶液中:c(H2A-)>c(Na+)>c(H+)>c(OH-)
B.25℃时,H3A的第二步电离平衡常数的数量级为10-5
C.b点溶液中:c(Na+)+c(H+)=3c(H2A-)+3c(A3-)+c(OH-)
D.当该溶液中c(HA2-)=c(A3-)时,溶液中水电离出的c(H+)>10-7molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒(V)、 锰(Mn)、铁(Fe)、 砷(As)、硒(Se)均为第四周期的元素,完成下列问题。
(1)钒有+2、+3、+4、+5等几种化合价。这几种价态中,最稳定的是______。
(2)基态Fe2+的价层电子的轨道表示式为________,检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______。
(3)部分电离能数据如下:
Mn:![]() =717kJ/mol ,
=717kJ/mol ,![]() =1509kJ/mol ,
=1509kJ/mol ,![]() =3248kJ/mol ,
=3248kJ/mol ,
Fe:![]() =759kJ/mol,
=759kJ/mol,![]() =1562kJ/mol ,
=1562kJ/mol ,![]() =2957kJ/mol ,
=2957kJ/mol ,
根据数据可知,气态Mn2+ 再失去一个电子比气态Fe2+ 再失去一个电子难,其原因是____________________。
(4)沸点:NH3__________AsH3(填“>”、“<”或“=”),原因是_____________________。
(5)H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3 酸性强的原因___________________________________ 。
(6)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下:
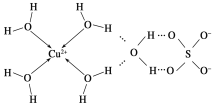
胆矾的化学式用配合物的形式表示为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香叶醇、橙花醇和乙酸橙花酯在工业上用作香料,它们可由月桂烯来合成。
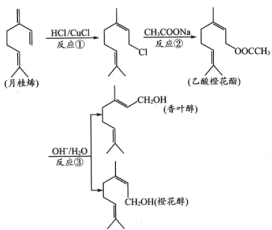
下列说法正确的是
A.反应①②③均为取代反应
B.月桂烯分子中所有碳原子全部处在同一平面上
C.香叶醇和橙花醇具有相同的分子式
D.乙酸橙花酯可以发生取代、加成、氧化和聚合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不饱和酯类化合物在药物、涂料等领域应用广泛。
(1)下列关于化合物Ⅰ的说法,正确的是___。

A.可能发生酯化反应和银镜反应
B.化合物Ⅰ含有5种官能团
C.1mol化合物Ⅰ在一定条件下最多能与7molH2发生加成反应
D.能与溴发生取代和加成反应
(2)下面反应是一种由烯烃直接制备不饱和酯的新方法。
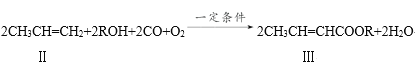
化合物Ⅲ与足量的NaOH溶液共热的化学方程式为__;反应类型是__。
(3)2—丁烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如下:
CH4+CO![]() CH3CHO(A)
CH3CHO(A)![]() B
B![]() CH3CH=CHCOOH(D)
CH3CH=CHCOOH(D)![]() E
E
已知:HCHO+CH3CHO![]() CH2=CHCHO+H2O
CH2=CHCHO+H2O
①B中官能团的名称为___。
②E的结构简式为___。
③试剂C可选用下列中的___。
a.溴水 b.银氨溶液 c.酸性KMnO4溶液 d.新制Cu(OH)2悬浊液
④B在一定条件下可以生成高聚物F,该反应的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.FeO与稀硝酸反应属于复分解反应
B.常温下Fe与浓硝酸不反应
C.铜片与浓硝酸发生离子反应:Cu+NO3-+4H+=Cu2++NO2↑+2H2O
D.向Fe(NO3)2稀溶液中加入盐酸发生反应:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示甲是某学生验证铜和浓硝酸反应的装置,乙、丙是另外两位同学对甲装置改进后的装置:

(1)甲、乙、丙三个装置中都发生的反应的化学方程式:__。
(2)和甲装置相比,乙装置的优点是
①__;
②__。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。实验时先关闭止水夹__,再打开止水夹__,才能使NO2气体充满②试管;当气体充满②试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入②试管,应该__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据图回答下列问题:

(1)若烧杯中的溶液为稀硫酸,则观察到的现象是___________,负极反应式为___________。
(2)若烧杯中的溶液为氢氧化钠溶液,则正极反应为___________,总反应的化学方程式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com