
【题目】[化学一选修5:有机化学基础]
聚对苯二甲酸丁二醇酯(PBT)是一种性能优异的热塑性高分子材料。PBT的一种合成路线如图所示:
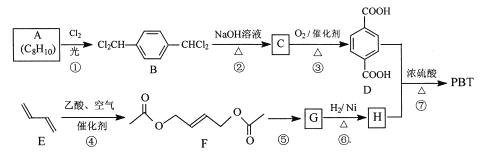
回答下列问题:
(1)A的结构简式是_________,C的化学名称是_________。
(2)⑤的反应试剂和反应条件分别是__________。
(3)F的分子式是_________,⑥的反应类型是_________。
(4)⑦的化学方程式是_________。
(5)M是H的同分异构体,同时符合_列条件的M可能的结构有_________种。
a.0.1 molM与足量金属钠反应生成氢气2.24 L(标准状况)
b.同一个碳原子上不能连接2个羟基
其中核磁共振氢谱显不3组峰,且峰而积之比为3:1:1的结构简式是_________。
(6)以2一甲基-1-3一丁二烯为原料(其它试剂任选),设计制备![]() 的合成路线:_________
的合成路线:_________
【答案】 ![]() 对苯二甲醛 NaOH溶液,加热(或H+/△) C8H12O4 加成反应(或还原反应)
对苯二甲醛 NaOH溶液,加热(或H+/△) C8H12O4 加成反应(或还原反应)  5
5 ![]()

或![]()
【解析】由![]() 可知A为:
可知A为:![]() ;由
;由![]() 可知C为:
可知C为: ;由
;由 以及 PBT为聚对苯二甲酸丁二醇酯可知G为:
以及 PBT为聚对苯二甲酸丁二醇酯可知G为:
![]() 、H为:
、H为:![]() ;根据以上分析可解答下列问题:
;根据以上分析可解答下列问题:
(1)A的结构简式是![]() ,C的结构简式是
,C的结构简式是 ,化学名称是对苯二甲醛。答案为:
,化学名称是对苯二甲醛。答案为: ![]() 、对苯二甲醛
、对苯二甲醛
(2)反应⑤是由F生成G的反应,属于酯的水解反应,所以反应试剂和反应条件分别是NaOH溶液,加热(或H+/△)。 答案为:NaOH溶液,加热(或H+/△)
(3)F的结构简式为:  ,所以分子式是C8H12O4,反应⑥是由
,所以分子式是C8H12O4,反应⑥是由![]() 生成
生成![]() 的反应,属于加成反应(或还原反应);答案为: C8H12O4 、加成反应(或还原反应)
的反应,属于加成反应(或还原反应);答案为: C8H12O4 、加成反应(或还原反应)
(4)反应⑦是由对苯二甲酸与1,4-丁二醇的缩聚反应,反应方程式为: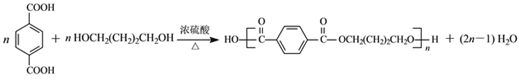
答案为:
(5)M是H的同分异构体,H为:HOCH2CH2CH2CH2OH,1molM与足量钠反应放出![]() 氢气,说明官能团为2个羟基;1个碳原子上不能连接2个羟基,分情况讨论,①当骨架为直链时,先确定一个羟基的位置,再判断另一个羟基的位置,如图:
氢气,说明官能团为2个羟基;1个碳原子上不能连接2个羟基,分情况讨论,①当骨架为直链时,先确定一个羟基的位置,再判断另一个羟基的位置,如图: 、
、,共4种,②当存在支链时:
 、
、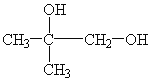 ,共2种,所以符合条件的有机化合物M共有6种,去掉H本身这一种还有5种,所以符合条件的M可能的结构有5种。其中核磁共振氢谱显示3组峰,且峰而积之比为3:1:1的结构简式为:
,共2种,所以符合条件的有机化合物M共有6种,去掉H本身这一种还有5种,所以符合条件的M可能的结构有5种。其中核磁共振氢谱显示3组峰,且峰而积之比为3:1:1的结构简式为:![]() 答案为:5 、
答案为:5 、![]()
(6)结合PBT的合成路线图,以及所学过的有机化学知识,由2一甲基-1-3一丁二烯为原料(其它试剂任选),制备![]() 的合成路线可以设计如下:
的合成路线可以设计如下:
或![]() 。
。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】用1 L 1.0 mol·L-1的氢氧化钠溶液吸收0.8 mol二氧化碳,所得溶液中碳酸根离子与碳酸氢根离子的物质的量浓度之比是 ( )
A.1∶3
B.1∶2
C.2∶3
D.3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以烃A和芳香烃D为原料合成化合物X的路线如图所示:

回答下列问题:
(1)A的名称是_______,F中含有的官能团名称是__________。
(2)E生成F的反应类型是___________。
(3)反应D→E的化学方程式为_______________________________。
(4)反应F→H的化学方程式为_________________________________。
(5)X的结构简式为________________,下列有关X的说法正确的是________(填字母)。
a.能发生水解反应 b.能发生银镜反应
c.不能使溴的四氯化碳溶液褪色 d.能与浓硝酸发生取代反应
(6)芳香族化合物M是G的同分异构体,M能与NaHCO3溶液反应产生气体,符合条件的M有_____种,其中核磁共振氢谱有6组峰且峰面积之比为1:2:2:2:2:1的是____________(填结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组称取纯净的Na2SO3 ·7H20 a克,隔绝空气加强热至恒重,经过分析与计算,得到的固体质量与全部转化为亚硫酸钠固体的计算值一致,但固体在水中溶解后测的pH值比理论计算值(相同浓度Na2SO3溶液的pH)大很多。下列说法不正确的是
A. 连续两次称量强热前后固体的质量,如质量差小于0.1g,即可判断固体已经恒重
B. 产生上述矛盾的可能解释:4Na2SO3 ![]() 3Na2SO4 + Na2S
3Na2SO4 + Na2S
C. 固体产物中加入稀盐酸可能有淡黄色沉淀产生
D. 加入BaCl2溶液,出现白色沉淀,则能确定产物中有Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了①~⑤五种元素在周期表中的位置:
ⅠA | O | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ||||||
请回答下列问题:
(1)写出以上五种元素对应的元素符号_______、_______、_______、_______、_______;
(2)②和③元素所形成的气态氢化物的稳定性由强到弱的顺序是(________)
A.前者大 B.后者大 C.相等 D.无法比较
(3)②元素的最高价氧化物的水化物呈(填“酸”、“碱”、“中”)_______性;
(4)②③两种元素的原子半径由大到小的顺序是(用元素符号表示)_______;
A.前者大 B.后者大 C.相等 D.无法比较
(5)①与⑤两种元素形成的化合物的化学式是_______;
(6)②与④两种元素的最高价氧化物的水化物在溶液中相互反应的化学方程式是____;
(7)写出①的氧化物含有的化学键类型_______,写出⑤的原子结构示意图_______;
(8)写出元素③处于第_______周期,第_______族;
(9)写出实验室制取⑤的单质的化学反应方程式_______;实验结束时,尾气处理应选择的试剂是_______溶液(化学式或名称);
(10)周期表中,同一主族从上往下原子半径_______,_______递增;周期表中,同一周期从左向右原子半径_______,_______递增。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是( )
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO | 稀硫酸 | 3Fe2++NO |
B | Fe3+、I-、ClO- | 氢氧化钠溶液 | Fe3++3OH-===Fe(OH)3↓ |
C | Ba2+、HCO | 氢氧化钠溶液 | HCO |
D | Al3+、Cl-、NO | 过量氢氧化钠溶液 | Al3++3OH-===Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料.某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下三种实验方案.
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
(1)(方案1)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去).

(i)图C装置中球形干燥管的作用是________.
完成以下实验步骤:组装好实验装置,首先进行的操作是________,再加入实验药品.接下来的实验操作是关闭,打开,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体.打开K1 ,通入氮气一段时间,测定C装置反应前后的质量变化.通入氮气的目的是________.
(iii)由于装置存在缺陷,导致测定结果偏高,请提出改进意见________.
(2)(方案2)用下图装置测定m g样品中A1N的纯度(部分夹持装置已略去).

(i)为测定生成气体的体积,量气装置中的X液体可以是________.
A.CCl4B.H2OC.NH4Cl溶液 D. ![]()
(ii)若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),则AlN的质量分数是________.
(3)(方案3)按以下步骤测定样品中A1N的纯度:

(i)步骤②生成沉淀的离子方程式为________.
(ii)若在步骤③中未洗涤,测定结果将________(填“偏高”、“偏低”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃A分子式为C8H10,它的主要用途是在石油化学工业作为生产苯乙烯的中间体,所制成的苯乙烯一般被用来制备常用的塑料制品——聚苯乙烯。某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色。J分子内有两个互为对位的取代基。在一定条件下各物质间有如下的转化关系:(无机物略去)

(1)A物质的名称为__________。写出核磁共振氢谱中只有2个特征峰的A的同分异构体的结构简式__________________。
(2)写出X的结构简式______________;J中所含的含氧官能团的名称为_________。
(3)E与H反应的化学方程式是_______________;反应类型是______________。
(4)B、C的混合物在NaOH 乙醇溶液中加热可以生成同一种有机物I,以I为单体合成的高分子化合物的结构简式是_________________。
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式________。
①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;
③苯环上的一卤代物有2种;④能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A. v(W)=3v(Z) B. 2v(X)=3v(Z)
C. 2v(X)=v(Y) D. 3v(W)=2v(X)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com