
| A. | CH4与C3H8 | B. | 苯与己烯 | C. | 己烷与苯 | D. | 苯与甲苯 |
 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 剩余固体的铁、铜混合物 | |
| B. | 反应后溶液中n(Fe3+)=0.10mol | |
| C. | 原固体混合物中铜的质量是9.6g | |
| D. | 反应后溶液中n(Fe2+)+n(Cu2+)=0.64mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气与氧气点燃生成水 | |
| B. | 硝酸银溶液中加入氯化钠溶液生成白色沉淀 | |
| C. | CuO与稀盐酸反应 | |
| D. | 二氧化碳使澄清石灰水变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素Y、Z、W形成的简单离子具有相同电子层结构,其离子半径依次增大 | |
| B. | X、Z、R三种元素构成的化合物中只含离子键 | |
| C. | 元素Z、R氧化物对应的水化物之间相互反应,生成的盐溶液只能呈中性 | |
| D. | 元素Y气态氢化物的稳定性强于元素R |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
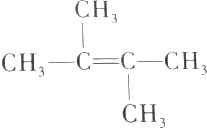 ,下列有关该烯烃分子的叙述中正确的是( )
,下列有关该烯烃分子的叙述中正确的是( )| A. | 该烯烃分子中的所有原子都在同一平面上 | |
| B. | 该烯烃分子中有4个碳原子可能在一条直线上 | |
| C. | 该烯烃分子中的6个碳原子不可能都在同一平面上 | |
| D. | 该烯烃与CH2=C(CH2CH3)2互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
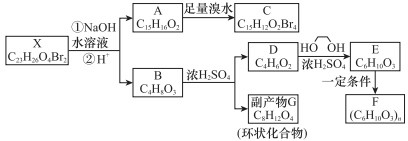
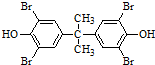 ,化合物C的1H-NMR谱的峰面积之比为1:2:3(按从小到大的顺序填写)
,化合物C的1H-NMR谱的峰面积之比为1:2:3(按从小到大的顺序填写) .
.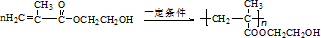 .
.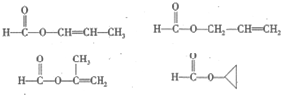 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g过氧化钠含有的共用电子对数为0.2NA | |
| B. | 过氧化氢使高锰酸钾溶液褪色,1mol过氧化氢得到2NA电子 | |
| C. | 在含有NH4+、Ba2+、Cl-、NO3-离子的溶液 加入过氧化钠以上各离子量几乎不减少 | |
| D. | 2H2O2(l)═2H2O(l)+O2(g);△H=-98.2 kJ/mol,△S=70.5 J/mol•K,该反应低温能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
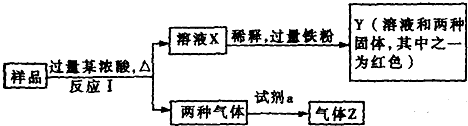
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由元素的原子序数推测其在元素周期表中的位置 | |
| B. | 由H-H和Cl-Cl的键长推测液氢和液氯沸点的高低 | |
| C. | 由CaF2晶体中,与Ca2+距离最近的F-有8个,推知与F-距离最近的Ca2+也有8个 | |
| D. | 由N≡N、H-H、N-H的键能数据估算3H2(g)+N2(g)?2NH3(g)的反应热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com