
将3摩A和2.5摩B混合于2升密闭容器中,发生如下反应:3A十B xC+2D。过5分钟后反应达平衡,这时生成1摩D,C的平均反应速度是0.1摩/(升·分)。下列说法错误的是:
xC+2D。过5分钟后反应达平衡,这时生成1摩D,C的平均反应速度是0.1摩/(升·分)。下列说法错误的是:
A.A的平均反应速度为0.15摩/(升·分) B. x值为1
C.B的平衡浓度为0.5摩/升 D. B的转化率为20%
科目:高中化学 来源: 题型:
下列关于物质分类的说法正确的是
A.金刚石、白磷都属于单质 B.漂白粉、石英都属于纯净物
C.氯化铵、次氯酸都属于强电解质 D.葡萄糖、蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表达正确的是( )
①活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同
②向100 mL0.1 mol/L的溴化亚铁溶液中通入0.05 mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
③斜长石KAlSi3O8的氧化物形式可表示为:K2O•Al2O3•3SiO2
④酸性条件下KIO3溶液与KI溶液发生反应生成I2时的离子方程式:
IO3-+5I-+3H2O=I2+6OH-
⑤碳酸氢根离子的电离方程式可表示为: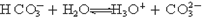

⑥元素周期表中,从上到下,卤族元素的非金属性逐渐减弱,氢卤酸的酸性依次减弱
⑦500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 
 2NH3(g) △H= 38.6 kJ·mol-1
2NH3(g) △H= 38.6 kJ·mol-1
A.全部 B.②⑤ C.②③④⑦ D.②④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
目前,全世界的镍消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍行业发展蕴藏着巨大的潜力。镍化合物中的三氧化二镍是一种重要的电子元件材料和二次电池材料。工业上可利用含镍合金废料(除镍外,还含有Fe、Cu、Ca、Mg、C等杂质)制取草酸镍,然后高温煅烧草酸镍来制取三氧化二镍。
已知:①草酸的钙、镁、镍盐均难溶于水,且溶解度:NiC2O4> NiC2O4·H2O> NiC2O4·2H2O
②常温下,Ksp[(Fe(OH))3]=4.0×10-38,lg5=0.7
根据下列工艺流程图回答问题:
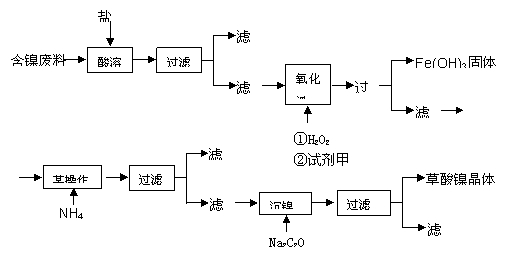

(1)加6%的H2O2时,温度不能太高,其目的是 。若H2O2在一开始酸溶时便与盐酸一起加入,会造成酸溶过滤后的滤液中增加一种金属离子,用离子方程式表示这一情况 。
(2)流程中有一步是调pH,使Fe3+转化为Fe(OH)3沉淀,常温下当溶液中c (Fe3+)=0.5×10-5mol/L时,溶液的pH= 。
(3)流程中加入NH4F的目的是 。
(4)将最后所得的草酸镍晶体在空气中强热到400℃,可生成三氧化二镍和无毒气体,写出该反应的化学方程式 。
(5)工业上还可用电解法制取三氧化二镍,用NaOH溶液调节NiCl2溶液的pH至7.5,再加入适量Na2SO4进行电解,电解产生的Cl2其80%的可将二价镍氧化为三价镍。写出Cl2氧化Ni(OH)2生成三氧化二镍的离子方程式 ;将amol二价镍全部转化为三价镍时,外电路中通过电子的物质的量是 。
(6)近年来镍氢电池发展很快,它可由NiO(OH)跟LaNi5H6(LaNi5H6中各元素化合价均可看作是零)组成:6NiO(OH)+LaNi5H6 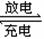 LaNi5+6Ni(OH)2。该电池放电时,负极反应是 。
LaNi5+6Ni(OH)2。该电池放电时,负极反应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
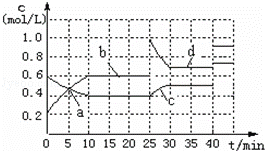
已知:2M(g)⇌ N(g);△H<0.现将M和N的混和
气体通入体积为1L的恒温密闭容器中,反应体系中各物质
的浓度随时间变化关系如图所示.下列说法正确的是:
|
| A. | a、b、c、d四个点中处于平衡状态的点是a、b |
|
| B. | 反应进行至25min时,曲线发生变化的原因是加入了 0.4mol N |
|
| C. | 若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
|
| D. | 若40min后出现如图所示变化,则可能是加入了某种催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃、101kPa 下:① 2Na(s)+1/2O2(g)= Na2O(s) △H1 =-414KJ/mol
② 2Na(s)+O2(g)= Na2O2(s) △H2 =-511KJ/mol 则下列说法正确的是:
A.等质量的钠分别发生反应①和②,产物的阴阳离子个数比相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25℃、101kPa 下,Na2O2(s)+2 Na(s)= 2Na2O(s) △H=-317kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质分类正确的是
A.液氯、冰水混合均为纯净物 B.NO2、CO、CO2均为酸性氧化物
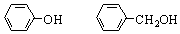 C. 与 互为同系物
C. 与 互为同系物
D.淀粉、纤维素和油脂都属于天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
氮氧化铝(AlON)是一种透明高硬度防弹材料,可以由反应Al2O3+C+N2=2AlON+CO(高温)合成,下列有关说法正确的是
A.氮氧化铝中氮的化合价是-3
B.反应中氮气作氧化剂
C.反应中每生成5.7g AlON 同时生成1.12 L CO
D.反应中氧化产物和还原产物的物质的量之比是2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com