
CO2 、SO2 、NOx 是对环境影响较大的气体,控制和治理CO2、SO2、NOx 是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx 浓度的有 (填字母)
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
(2)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。写出用合成气(CO和H2)生产甲醇的化学方程式 ,已知该反应合成1 mol液态甲醇吸收热量131.9 kJ, 2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g) △H =-594.1 kJ·mol-1,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式 。
(3)有人设想以下图所示装置用电化学原理将CO2、SO2 转化为重要化工原料。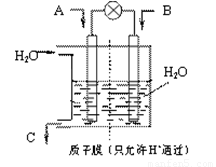
若A为CO2,B为H2,C为CH3OH,则通入CO2 的一极为 极;若A为SO2,B为O2,C为H2SO4。则负极的电极反应式为 ;
(4)①在研究氮的氧化物的转化时,某小组查阅到以下数据:17℃、1.01×105 Pa时,
2NO2(g)
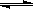 N2O4(g) △H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4
和NO2的混合气体达到平衡时,若 c (NO2)
= 0.0300 mol·L-1,
N2O4(g) △H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4
和NO2的混合气体达到平衡时,若 c (NO2)
= 0.0300 mol·L-1,
c (N2O4)= (保留两位有效数字);
②改变上述体系的某个条件,达到新的平衡后,测得混合气体中 c (NO2) = 0.04 mol·L-1, c (N2O4) = 0.007 mol·L-1,则改变的条件为 ;
(1)acd (2分)
(2)CO+2 H2=CH3OH(2分)
2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH =-1452 kJ·mol-1(3分)
(3)正(1分); SO2 +2H 2O-2e— = SO42-+ 4H+ (2分) ;
(4)①0.012 mol·L-1 (2分) ②升高温度(2分)
【解析】(1)使用无氟冰箱,减少氟里昂排放,是抑制臭氧层破坏的,b不正确,其余都是正确的,答案选acd。
(2)根据已知的反应物和生成物可知,方程式为CO+2H2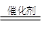 CH3OH。反应①CO(g)+2H2(g)
CH3OH。反应①CO(g)+2H2(g)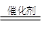 CH3OH(l)
△H =+131.9 kJ·mol-1,和反应②2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g) △H =-594.1 kJ·mol-1,所以根据盖斯定律可知,(②-①)×2即得到
2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g),所以反应热△H =(-594.1
kJ·mol-1-131.9
kJ·mol-1)×2=-1452 kJ·mol-1。
CH3OH(l)
△H =+131.9 kJ·mol-1,和反应②2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g) △H =-594.1 kJ·mol-1,所以根据盖斯定律可知,(②-①)×2即得到
2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g),所以反应热△H =(-594.1
kJ·mol-1-131.9
kJ·mol-1)×2=-1452 kJ·mol-1。
(3)在反应中碳元素的化合价降低,所以CO2是氧化剂,得到电子,因此CO2在正极通入。SO2失去电子,在负极通入,电极反应式为SO2 +2H 2O-2e— = SO42-+ 4H+ 。
(4)①根据平衡常数表达式可知,c (N2O4)=13.3×0.03002=0.012 mol·L-1。
②此时平衡常数是0.007÷0.042=4.375,即平衡常数减小。由于正反应是放热反应,所以改变的条件是升高温度,平衡向逆反应方向移动。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 欲提纯的物质与杂质 | 所选试剂 |
| Fe2O3(Al2O3)固体 | C C |
| Na2CO3(NaHCO3)固体 | E E |
| FeCl2( FeCl3)溶液 | A A |
| CO2(SO2)气体 | B B |
| SiO2(CaCO3)固体 | D D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某校化学兴趣小组在实验里制取乙烯时,加热时,因温度过高而发生副反应,部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气和炭黑.
某校化学兴趣小组在实验里制取乙烯时,加热时,因温度过高而发生副反应,部分乙醇跟浓H2SO4反应生成SO2、CO2、水蒸气和炭黑.
| ||
| ||
| 选用的仪器(填字母) | 加入的试剂 | 作用 |
| C | 浓H2SO4和乙醇 | 反应器(或发生气体) |
B B |
无水CuSO4 无水CuSO4 |
检验H2O 检验H2O |
A A |
品红溶液 品红溶液 |
检验SO2 检验SO2 |
A A |
酸性KMnO4溶液 酸性KMnO4溶液 |
吸收余下的SO2 吸收余下的SO2 |
A A |
澄清石灰水 澄清石灰水 |
检验CO2的存在 检验CO2的存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
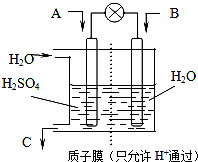 控制和治理CO2、SO2是解决温室效应、减少酸雨的有效途径,有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料.请回答:
控制和治理CO2、SO2是解决温室效应、减少酸雨的有效途径,有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质(杂质) | 除杂方法 | |
| A | Cl2(HCl) | 将气体通过盛有氢氧化钠溶液的洗气瓶 |
| B | CO2(SO2) | 将气体通过盛有饱和碳酸钠溶液的洗气瓶 |
| C | CaCO3(SiO2) | 加入足量盐酸后过滤 |
| D | Mg(Al) | 加入足量氢氧化钠溶液后过滤 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com