
 在稀氨水中,丁二酮肟(CH3C=N-OH)2与Ni2+反应可生成鲜红色沉淀丁二酮肟镍(结构如图),常用于检验Ni2+.
在稀氨水中,丁二酮肟(CH3C=N-OH)2与Ni2+反应可生成鲜红色沉淀丁二酮肟镍(结构如图),常用于检验Ni2+.分析 碳氮之间是双键,双键是由一个σ键和一个π键构成;镍原子有空轨道,氮原子有孤电子对,因此二者形成配位键;丁二酮肟中甲基中的碳原子都是单键,在与氮相连的碳上有碳氮双键,以此解答该题.
解答 解:①由结构简式可知分子中存在配位键,含有C=N键,则含有σ键、π键、氧氢之间除共价键外还可存在氢键,分子中不含离子键和金属键,
故答案为:ACDF;
②丁二酮肟中甲基中的碳原子都是单键,在与氮相连的碳上有碳氮双键,因此杂化类型是sp2和sp3杂化,故答案为:sp2、sp3.
点评 本题考查晶体的结构与物质的性质的相互关系及应用,为高频考点,侧重考查学生的分析能力,做题时注意化学键的识别以及杂化类型的判断,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 2-甲基戊烷和4-甲基戊烷互为同分异构体 | |
| B. | 分子式为C5H10O2且能与NaHCO3反应的有机物有3种 | |
| C. | 乙醇制备乙烯和乙醇制备乙酸乙酯均为脱水的取代反应 | |
| D. | 苯与液溴在FeBr3作催化剂的条件下发生取代反应,生成溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①②③④均可与Na、NaOH、H2发生反应,1mol四种物质最多消耗Na、NaOH、H2的物质的量之比依次分别为1:1:1:1、1:2:2:1、4:3:3:5 | |
| B. | ①②③④属同分异构体,分子式为C8H8O3 | |
| C. | 可用银氨溶液或酸性KMnO4溶液区分③④ | |
| D. | ①②③④中所有原子均不可能处于同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )
含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )| A. | 对乙酰氨基酚的分子式为:C8H10NO2 | |
| B. | 对乙酰氨基酚可与浓溴水发生加成反应 | |
| C. | 与对乙酰氨基酚互为同分异构体,分子中含有硝基和苯环,且苯环上有三个取代基的分子共有6种 | |
| D. | 对乙酰氨基酚可以与Na2CO3发生反应,产生CO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeAl合金 | B. | ZnAl合金 | C. | CuMg合金 | D. | MgAl合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
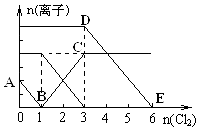 已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )
已知:2Fe3++2I-=2Fe2++I2,向1L含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.横、纵坐标的单位均为mol.有关说法不正确的是( )| A. | 线段BC代表Fe3+ 物质的量的变化情况 | |
| B. | 原混合溶液中c(FeBr2)=6 mol/L | |
| C. | 当通入Cl22mol时,溶液中已发生的反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- | |
| D. | 原溶液中n (Fe2+):n (I-):n(Br-)=2:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
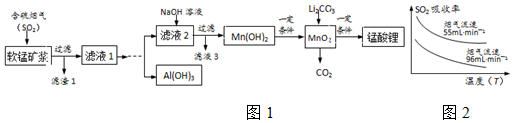
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 3.4 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 4.7 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2CO3(NH4Cl):加热 | |
| B. | CO2(SO2):饱和碳酸钠溶液、浓硫酸,洗气 | |
| C. | KCl溶液(BaCl2):加入适量K2SO4溶液,过滤. | |
| D. | 蛋白质(葡萄糖):浓Na2SO4溶液,盐析、过滤、洗涤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com