
 .
. )的衍生物,且取代基都在同一个苯环上;
)的衍生物,且取代基都在同一个苯环上;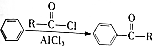 (R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和
(R为烃基).根据已有知识并结合相关信息,写出以ClCH2CH2CH2Cl和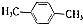 为原料制备
为原料制备 的合成路线流程图(无机试剂可任选).合成路线流程图示例如图所示:
的合成路线流程图(无机试剂可任选).合成路线流程图示例如图所示: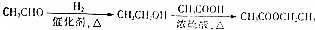
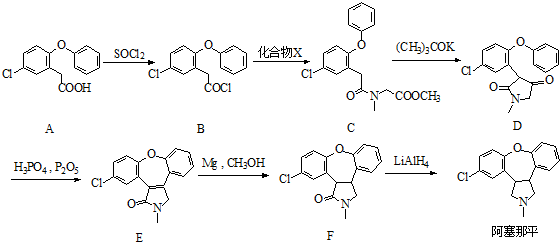
分析 (1)由A的结构简式,可知含有的含氧官能团有羧基、醚键;
(2)对比B、C的结构可知B发生取代反应生成C,结合X的分子式确定其结构简式;
(3)D到E的转化中先是苯环与羰基发生加成反应,然后醇羟基发生消去反应形成碳碳双键;
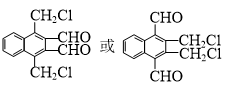
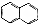
(4)时满足下列条件的B的一种同分异构体:Ⅰ.是萘(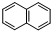 )的衍生物,且取代基都在同一个苯环上,Ⅱ.分子中所有碳原子一定处于同一平面,碳原子均与苯环相连符合,Ⅲ.能发生银镜反应,说明含有醛基,再结合分子中含有4种不同化学环境的氢书写;
)的衍生物,且取代基都在同一个苯环上,Ⅱ.分子中所有碳原子一定处于同一平面,碳原子均与苯环相连符合,Ⅲ.能发生银镜反应,说明含有醛基,再结合分子中含有4种不同化学环境的氢书写;
(5)ClCH2CH2CH2Cl发生水解反应得到HOCH2CH2CH2OH,再发生氧化反应生成OHCCH2CHO,进一步氧化生成HOOCCH2COOH,再与SOCl2反应生成 ,最后与对二甲苯反应得到
,最后与对二甲苯反应得到 .
.
解答 解:(1)由A的结构简式可知含有的含氧官能团有羧基、醚键,
故答案为:羧基、醚键;
(2)对比B、C的结构可知B发生取代反应生成C,X的分子式为C4H9NO2,则其结构简式为CH3NHCH2COOCH3,
故答案为:CH3NHCH2COOCH3;
(3)D到E的转化中先是苯环与羰基发生加成反应,然后醇羟基发生消去反应形成碳碳双键,
故答案为:消去;
(4)时满足下列条件的B的一种同分异构体:Ⅰ.是萘( )的衍生物,且取代基都在同一个苯环上,Ⅱ.分子中所有碳原子一定处于同一平面,碳原子均与苯环相连符合,Ⅲ.能发生银镜反应,说明含有醛基,且分子中含有4种不同化学环境的氢,符合条件的同分异构体为:
)的衍生物,且取代基都在同一个苯环上,Ⅱ.分子中所有碳原子一定处于同一平面,碳原子均与苯环相连符合,Ⅲ.能发生银镜反应,说明含有醛基,且分子中含有4种不同化学环境的氢,符合条件的同分异构体为: ,
,
故答案为: ;
;
(5)ClCH2CH2CH2Cl发生水解反应得到HOCH2CH2CH2OH,再发生氧化反应生成OHCCH2CHO,进一步氧化生成HOOCCH2COOH,再与SOCl2反应生成 ,最后与对二甲苯反应得到
,最后与对二甲苯反应得到 ,合成路线流程图为:
,合成路线流程图为: ,
,
故答案为: .
.
点评 本题考查有机物的合成、有机反应类型、官能团的结构、限制条件同分异构体书写等,侧重考查学生分析推理能力,熟练掌握官能团的性质与转化,注意对题目信息的利用.


科目:高中化学 来源: 题型:解答题
 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:①X元素原子价电子排布式为ns2np3,且原子半径是同族元素中最小的.②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有一个未成对电子.③Z元素的电离能数据如表(kJ/mol):
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:①X元素原子价电子排布式为ns2np3,且原子半径是同族元素中最小的.②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有一个未成对电子.③Z元素的电离能数据如表(kJ/mol):| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
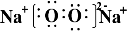 ,含有的化学键类型为离子键、非极性键,Z2Y2为离子晶体、
,含有的化学键类型为离子键、非极性键,Z2Y2为离子晶体、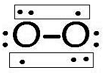 ,其分子空间构型为直线型.
,其分子空间构型为直线型.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 序号 | 实验操作示意图 | 实验现象 |
| Ⅰ | 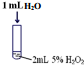 | 有极少量气泡产生 |
| Ⅱ | 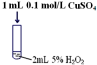 | 产生气泡速率略有加快 |
| Ⅲ | 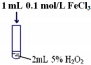 | 产生气泡速率明显加快 |
| t/min | 0 | 2 | 3 | 6 | 8 | 10 |
| v(O2)mL | 0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8 mol | B. | 3.6 mol | C. | 100 mol | D. | 200 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | L层上的电子数为奇数的原子一定是主族元素的原子 | |
| B. | 元素周期表中只有第IIA元素的原子最外层有两个电子 | |
| C. | 元素周期表中第Ⅷ族分占8、9、10三列,是元素种类最多的一族 | |
| D. | 元素周期表中位于金属和非金属交界线附近的元素属于过渡元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述反应中每生成1mol N2O,消耗67.2LCO | |
| B. | 等质量的N2O和CO2含有相等的电子数 | |
| C. | N2O只有氧化性,无还原性 | |
| D. | 上述反应中若有3 mol的CO被还原,则转移6NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com