
【题目】一定温度下,将3molA气体和1molB气体通入某密闭容器中,发生如下反应:![]() 。请回答下列问题:
。请回答下列问题:
(1)若容器体积固定为2L
①反应1min时测得剩余1.8mol A,C的浓度为0.4mol/L.1min内,B的平均反应速率为 ____________;x= ________
②若反应2min达到平衡,平衡时C的浓度 ______ (填“大于”“等于”或“小于”)0.8mol/L
③平衡混合物中,C的体积分数为22%,则A的转化率是 ______ ![]() 保留3位有效数字
保留3位有效数字![]()
(2)一定温度下,可逆反应:![]() 在体积固定的密闭容器中反应,达到平衡状态的标志是 ______
在体积固定的密闭容器中反应,达到平衡状态的标志是 ______
①单位时间内生成nmolO2,同时生成2nmolNO
②用NO、O2、NO2的物质的量浓度变化表示的反应速率的比:2:1:2
③混合气体的密度不随时间的变化而变化
④O2的物质的量浓度不变
【答案】0.2mol/(Lmin) 2 小于 36.1% ④
【解析】
(1)利用三段式法计算
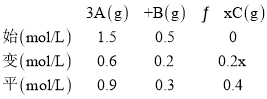
0.2x=0.4,x=2,以此解答该题;
(2)平衡标志是正逆反应速率相同,各组分含量保持不变分析选项。
(1)利用三段式法计算:

①1min内,B的平均反应速率为v(B)=![]() =0.2mol/(Lmin),0.2x=0.4,x=2;
=0.2mol/(Lmin),0.2x=0.4,x=2;
②随着反应的进行,反应速率逐渐减小,若反应经2min达到平衡,反应速率应小于1min时的速率,则1min时,C的浓度为0.4mol/L,则则平衡时C的浓度小于0.8mol/L;
③平衡混合物中,C的体积分数为22%,设转化了3xmolA,则有:

![]() ×100%=22%,x=0.361,则A的转化率是
×100%=22%,x=0.361,则A的转化率是![]() ×100%=36.1%;
×100%=36.1%;
(2)一定温度下,可逆反应:2NO(g)+O2(g)2NO2(g)在体积固定的密闭容器中反应;
①单位时间内生成n mol O2,同时生成2n mol NO,说明反应逆向进行,不能说明反应达到平衡状态,故①错误;
②用NO、O2、NO2的物质的量浓度变化表示的反应速率的比在反应过程中和平衡状态始终为2:1:2,不能说明反应达到平衡状态,故②错误;
③反应前后气体质量和体积始终不变,混合气体的密度不随时间的变化而变化,不能说明反应达到平衡状态,故③错误;
④O2的物质的量浓度不变是平衡标志,故④正确;
故答案为④。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】芳香族化合物A1和A2分别和浓H2SO4在一定温度下共热都只生成烃B,B的蒸气密度是同温同压下H2密度的59倍,B苯环上的一硝基取代物有三种,有关物质之间的转化关系如下:
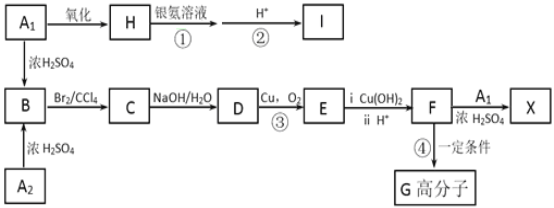
⑴D的分子式为_________________,I中官能团结构简式为_______________________,反应④的反应类型为________________。
⑵写出下列物质的结构简式:A2___________________;X __________________。
⑶写出下列反应的化学方程式:①_______________________________。
⑷化合物J是比化合物E多一个碳原子的E的同系物,化合物J有多种同分异构体,其中同时满足下列条件的同分异构体有___________________种;
①苯环上有两个取代基; ②能使FeCl3溶液显色; ③与E含有相同官能团
写出其中核磁共振氢谱图中峰面积比为1:1:2:2:6的结构简式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①相同质量的SO2、SO3的物质的量之比为________;
②氧原子的个数之比为________。
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为________,R的相对原子质量为________。含R的质量为1.6 g的Na2R,其物质的量为________。
(3)相同条件下10mLA2气体与30mLB2气体恰好完全反应生成20mL某气体C,则C的化学式为__________________(用A、B表示),推断中用到的原理理论是:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2A(g) + 3B(g) ![]() 2C(g)+D(g),在四种不同条件下的反应速率分别为:
2C(g)+D(g),在四种不同条件下的反应速率分别为:
①υ(A)=0.5mol·L-1·min-1 ②υ(B)=0.6 mol·L-1·min-1
③υ=0.35 mol·L-1·min-1 ④υ(D)=0.4 mol·L-1·min-1
该反应在这四种不同条件下反应速率由快到慢的顺序是
A. ①②③④ B. ②①④③ C. ④①②③ D. ②④①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )
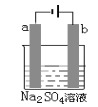
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图装置中的变化叙述错误的是
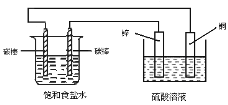
A.电子经导线从锌片流向右侧碳棒,再从左侧碳棒流回铜片
B.铜片上发生氧化反应
C.右侧碳棒上发生的反应:2H++2e→H2 ↑
D.铜电极出现气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置中,甲池的总反应式为2CH3OH+ 3O2+ 4KOH=2K2CO3+ 6H2O。试回答:
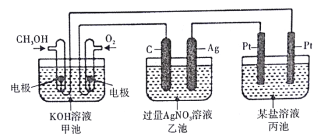
(1)图中甲池的装置是_________(填“原电池”或“电解池”),乙池中石墨电极是________极。
(2)写出通入CH3OH的电极的电极反应式:________________
(3)乙池中总反应的化学方程式为___________________
(4)当乙池中Ag极的质量增加5.40g时,甲池中理论上消耗O2________mL(标准状况);此时丙池某电极上析出1.60g某金属,则丙池中的盐溶液可能是________(填字母)
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一绝热(不与外界发生热交换)的恒容容器中,发生反应:2A(g)+B(s) ![]() C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
①容器内温度不变 ②混合气体的密度不变 ③混合气体的压强不变
④混合气体的平均相对分子质量不变 ⑤C(g)的物质的量浓度不变
⑥容器内A、C、D三种气体的浓度之比为2:1:1 ⑦某时刻v(A)=2v(C)且不等于零
⑧单位时间内生成n mol D,同时生成2n mol A
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有①6.72 L CH4;②3.01×1023个HCl分子;③7.2 g H2O,下列对这三种物质的关系从小到大的排列顺序是:
(1)物质的量______;
(2)体积______;
(3)质量______;
(4)氢原子数______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com