
| A.2,4,3,2,2,6 | B.0,2,1,0,1,2 |
| C.2,0,1,2,0,2 | D.2,8,5,2,4,10 |
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源:不详 题型:填空题

| A.为下一步反应提供碱性的环境 |
| B.使KClO3转化为KClO |
| C.与溶液I中过量的Cl2继续反应,生成更多的KClO |
| D.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Sb4O6+6FeS②Sb4O6+6C
Sb4O6+6FeS②Sb4O6+6C 4Sb+6CO↑,关于反应①、②的说法正确的是( )
4Sb+6CO↑,关于反应①、②的说法正确的是( )A.反应①②中的氧化剂分别是 、 、 |
| B.反应①中每生成1mol FeS时,共转移3mol电子 |
| C.反应②说明高温下C的还原性比Sb强 |
| D.每生成4mol Sb时,反应①与反应②中还原剂的物质的量之比为4:3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.与NaOH反应的氯气一定为0.3 mol |
| B.反应后的溶液中n(Na+):n(Cl-)可能为7:3 |
| C.若反应中转移的电子为n mol,则0.15<n<0.25 |
| D.n(NaCl):n(NaClO):n(NaClO3)可能为11﹕2﹕1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
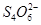 +2H2O下列说法中,不正确的是 ( )
+2H2O下列说法中,不正确的是 ( )| A.S2O32-是还原剂 | B.Y的化学式为Fe2O3 |
| C.a=4 | D.每有1mol O2参加反应,转移的电于总数为4 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法中正确的是
2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法中正确的是| A.KClO3在反应中是还原剂 |
| B.1 mol KClO3参加反应,在标准状况下能得到22.4 L气体 |
| C.在反应中H2C2O4既不是氧化剂也不是还原剂 |
| D.1 mol KClO3参加反应有1 mol电子转移 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.+2 | B.+3 | C.+4 | D.+6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3∶1 | B.2∶1 | C.15∶2 | D.1∶1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com