
(��)FeCl3��ˮ��Һ��________(����ԡ��������ԡ������ԡ�)��ԭ����________(�����ӷ���ʽ��ʾ)��ʵ��������FeCl3��ˮ��Һʱ������FeCl3���������ڽ�Ũ�������У�Ȼ����������ˮϡ�͵������Ũ�ȣ���________(��ٽ����������ơ�)��ˮ�⣻�����FeCl3��Һ���ɣ����գ����õ�����Ҫ���������________��
(��)ij������ȤС�����ⶨijNaOH��Һ��Ũ�ȣ�������������£�
����0.10 mol/L�ı�������ϴ��ʽ�ζ���2��3��
��ȡ������ע����ʽ�ζ�������0���̶�����2��3 mL��
�۰�ʢ�б��������ʽ�ζ��̶ܹ��ã����ڵζ��ܼ���ʹ֮������Һ
�ܵ���Һ������0����0���̶����£����¶���
��ȡ20.00 mL����NaOH��Һע��ྻ����ƿ�У�������2��3�μ�����Һ
�ް���ƿ���ڵζ��ܵ����棬�ñ�����ζ����յ㣬��¼�ζ��ܶ���
��ش��������⣺
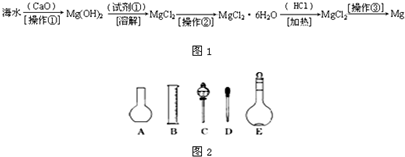
(1)ij�εζ�ʱ�ĵζ����е�Һ������ͼ��ʾ�������Ϊ ________mL��

(2)�����������ݣ�

���������ռ���Һ��Ũ��Ϊ________mol/L��
(3)����ʵ�������ʹʵ����ƫ�ߵ���________��
A����ƿ�ô���Һ��ϴ����ע�����Һ
B����ʽ�ζ���δ�ñ�Һ��ϴ����װ���Һ
C����ʽ�ζ��ܵζ�ǰ���Ӷ������ζ������Ӷ���
D����ʽ�ζ��ܵζ�ǰ�����ݣ��ζ���������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
| 162.5cV |
| m |
| 162.5cV |
| m |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| 1 |
| 2 |
| 3 |
| 2 |
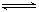 2CO2��ƽ�ⳣ��ΪK1����Ӧ4Fe+3O2
2CO2��ƽ�ⳣ��ΪK1����Ӧ4Fe+3O2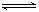 2Fe2O3��ƽ�ⳣ��K2����Ӧ3CO+Fe2O3
2Fe2O3��ƽ�ⳣ��K2����Ӧ3CO+Fe2O3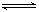 2Fe+3CO2��ƽ�ⳣ��K��K1��K2�Ĺ�ϵʽ
2Fe+3CO2��ƽ�ⳣ��K��K1��K2�Ĺ�ϵʽ
|
|
| ||
| ||
| n(C) |
| n(Fe2O3) |
| n(C) |
| n(Fe2O3) |
| n(C) |
| n(Fe2O3) |
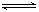 HSO3-+OH-
HSO3-+OH-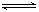 HSO3-+OH-
HSO3-+OH-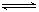 2AlCl3��g��+3CO��g����H��0������߽��������Ȼ�Ч�������ɲ�ȡ�Ĵ�ʩ��
2AlCl3��g��+3CO��g����H��0������߽��������Ȼ�Ч�������ɲ�ȡ�Ĵ�ʩ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 Fe��OH��3����+3HCl
Fe��OH��3����+3HCl Fe��OH��3����+3HCl
Fe��OH��3����+3HCl�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com