
 xC(g)��2D(g)�� 2 min��÷�Ӧ�ﵽƽ�⣬����0.8 mol D�������C��Ũ��Ϊ0.2 mol��L��1���������ж���ȷ����
xC(g)��2D(g)�� 2 min��÷�Ӧ�ﵽƽ�⣬����0.8 mol D�������C��Ũ��Ϊ0.2 mol��L��1���������ж���ȷ���� | A��x��2 |
| B��2 min��A�ķ�Ӧ����Ϊ0.6 mol��L��1��min��1 |
| C��B��ת����Ϊ40% |
| D�������������ܶȲ��䣬������÷�Ӧ�ﵽƽ��״̬ |
 â���̸����������������ϵ�д�
â���̸����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
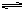 2NH3 ��H=" -" 92.4kJ/mol
2NH3 ��H=" -" 92.4kJ/mol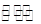 2NO2(g) ��H��0��ϵ�У����ɷ�Ũ����ʱ��ı仯��ͼ��
2NO2(g) ��H��0��ϵ�У����ɷ�Ũ����ʱ��ı仯��ͼ��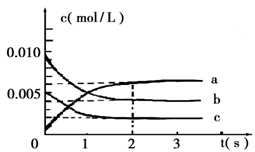
 4CO2(g)��N2(g) ��H����1 200 kJ��mol��1���ڸ÷�Ӧ���¶Ȳ�ͬ(T2>T1)������������ͬʱ������ͼ����ȷ����______(�����)��
4CO2(g)��N2(g) ��H����1 200 kJ��mol��1���ڸ÷�Ӧ���¶Ȳ�ͬ(T2>T1)������������ͬʱ������ͼ����ȷ����______(�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2HBr(g)����H<0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����仯��ϵ��ͼ��ʾ������˵����ȷ����
2HBr(g)����H<0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����仯��ϵ��ͼ��ʾ������˵����ȷ����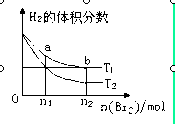
| A����ͼ��֪��T2>T1 |
| B��a��b����ķ�Ӧ���ʣ�b>a |
| C��Ϊ�����Br2(g)��ת���ʣ��ɲ�ȡ����Br2(g)ͨ�����ķ��� |
| D��T1ʱ������Br2(g)���룬ƽ��ʱHBr����������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3OH(g) �������������䣬��300���500��ʱ�����ʵ���n(CH3OH)-��Ӧʱ��t�ı仯������ͼ��ʾ������˵����ȷ����
CH3OH(g) �������������䣬��300���500��ʱ�����ʵ���n(CH3OH)-��Ӧʱ��t�ı仯������ͼ��ʾ������˵����ȷ����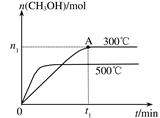
| A���÷�Ӧ�ġ�H��0 |
| B�������������䣬�����¶ȷ�Ӧ��ƽ�ⳣ������ |
C��300��ʱ��0-t 1min�� CH3OH��ƽ����������Ϊ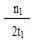 mol·L��1 min��1 mol·L��1 min��1 |
D��A��ķ�Ӧ��ϵ��300�����ߵ�500�棬�ﵽƽ��ʱ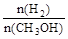 ��С ��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
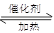 7N2(g)��12 H2O(g)�ɴ���NO2��700��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������NO2��NH3, ��Ӧ�����вⶨ�IJ������ݼ��±�
7N2(g)��12 H2O(g)�ɴ���NO2��700��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������NO2��NH3, ��Ӧ�����вⶨ�IJ������ݼ��±�| ��Ӧʱ��/min | n(NO2)/mol | n(NH3)/ mol |
| 0 | 1��20 | 1��60 |
| 2 | 0��90 | |
| 4 | | 0��40 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NO2(g)��ƽ�⡣��ͼ��ʾ�ⶨN2O4��Ũ����ʱ���ϵ�����ߣ�������ΪN2O4��Ũ�ȣ�������Ϊʱ�䣩��
2NO2(g)��ƽ�⡣��ͼ��ʾ�ⶨN2O4��Ũ����ʱ���ϵ�����ߣ�������ΪN2O4��Ũ�ȣ�������Ϊʱ�䣩��
|
| T/K | 310 | 320 |
| Kֵ | 0.38 | 0.42 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 cC(g)+dD(g)���ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽ��ƽ��ʱ��D��Ũ��Ϊԭ����1��8��������˵����ȷ����
cC(g)+dD(g)���ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽ��ƽ��ʱ��D��Ũ��Ϊԭ����1��8��������˵����ȷ����| A���ڢ� | B���٢� | C���ۢ� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)+Q��Q>0��������������Ũ����ʱ��仯��������ͼ��ʾ������˵������ȷ����
2C(g)+Q��Q>0��������������Ũ����ʱ��仯��������ͼ��ʾ������˵������ȷ����
| A��30minʱ�����¶ȣ�40minʱ�����¶� |
| B��40min��54min֮�䷴Ӧ����v(��) < v(��) |
| C����20min��30minʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1 >K2 |
| D��0~8minA��ƽ����Ӧ����Ϊ0��64mol/(L��min) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2Cl2+2H2O����ʵ���ȵ�ѭ�����á�
2Cl2+2H2O����ʵ���ȵ�ѭ�����á�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com