
| A. |  | B. |  | C. | 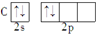 | D. |  |
分析 能量最低原理:原子核外电子先占有能量较低的轨道.然后依次进入能量较高的轨道.
保里不相容原理:每个原子轨道上最多只能容纳2个自旋状态相反的电子.
洪特规则:原子核外电子在能量相同的各个轨道上排布时①电子尽可能分占不同的原子轨道,②自旋状态相同,③全空、全满或半满时能量最低.
解答 解:A、N原子核外电子数为7,处于2p能级上的3个电子应尽可能分占3个不同2p原子轨道,且自旋状态相同,因此违背了洪特规则,故A错误;
B、O原子核外电子数为8,处于2p能级上的4个电子应尽可能分占3个不同2p原子轨道,且自旋状态相同,因此违背了洪特规则,故B错误;
C、C原子核外电子数为6,处于2p能级上的2个电子应尽可能分占3个不同2p原子轨道,且自旋状态相同,因此违背了洪特规则,故C错误;
D、F原子核外电子数为9,处于2p能级上的5个电子符合保里不相容原理和洪特规则,故D正确;
故选D.
点评 本题考查了原子核外电子排布,领会能量最低原理、保里不相容原理、洪特规则的内容来是答题的关键,难度不大.


科目:高中化学 来源: 题型:解答题
| 编号 | 混合物 | 试剂序号 | 方法序号 |
| (1) | 硝酸钾和氯化钠的固体混合物 | ||
| (2) | 氯化钾和碘的混合溶液 | ||
| (3) | 汽油和水的混合物 | ||
| (4) | 乙二醇(沸点198℃)和丙三醇(沸点290℃)的混合物 | . |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锅炉中沉积的水垢大部份可以用稀盐酸溶解去除 | |
| B. | 加热FeCl3饱和溶液制备Fe(OH)3促进了Fe3+水解 | |
| C. | 向纯水中加入盐酸或降温都能使水的离子积减小,水的电离平衡都逆向移动 | |
| D. | 反应2A(g)+B(g)═3C(s)+D(g)在一定条件下能自发进行,说明该反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2的电子式: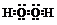 | |
| B. | 乙醇的结构式:C2H6O | |
| C. | 磷原子的结构示意图: | |
| D. | FeSO4 的电离方程式:FeSO4=Fe3++SO42ˉ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应后生成的盐只有Fe(NO3)2 | B. | 反应后生成的盐只有Fe(NO3)3 | ||
| C. | 反应后生成的盐为Fe(NO3)2和Fe(NO3)3 | D. | 以上三种情况都有可能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖的分子式:C6H12O6 | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 14C的原子结构示意图: | D. | 氯气的电子式:Cl:Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com