
 互为同分异构体的是( )
互为同分异构体的是( )A、 |
B、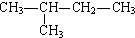 |
C、 |
D、 |
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:
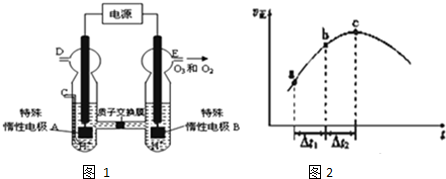
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶的体积标线刻在瓶颈上 |
| B、量筒的“0“标线在中间 |
| C、量筒最下端刻有“0“标线 |
| D、托盘天平刻度尺有“0“标线,刻在尺的中间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| HCl |
| NaOH/H2O |
| △ |
| O2(Cu) |
| △ |
| HCN |
| 加成 |
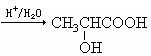
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯和溴水振荡后,由于发生化学反应而使溴水的水层颜色变浅 |
| B、酸性高锰酸钾溶液和溴水都既能鉴别出甲烷和乙烯又能除去甲烷中含有的乙烯再经干燥而获得纯净的甲烷 |
| C、煤中含有苯和甲苯,可以用先干馏,后蒸馏的方法把它们分离出来 |
| D、石油中含有C5~C11的烷烃,可以通过分馏得到汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:
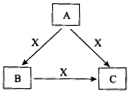 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.若A、B、C的焰色反应均呈黄色,水溶液均为碱性.
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.若A、B、C的焰色反应均呈黄色,水溶液均为碱性.查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol?L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.160 |
| c(S2O82-/mol?L-1) | 0.040 | 0.040 | 0.080 | 0.080 | 0.040 |
| t/s | 88 | 44 | 22 | 11 | t1 |
| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钠(s) |
| B、硫酸钠(s) |
| C、醋酸钠(s) |
| D、硫酸铵(s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com