
| A. | Na、Mg、Al的还原性依次减弱 | B. | I、Br、Cl的非金属性性依次增强 | ||
| C. | C、N、O 的原子半径依次增大 | D. | P、S、Cl的最高正化合价依次升高 |
分析 A.元素的金属性越强,对应的单质的还原性越强;
B.元素的非金属性越强,对应单质的氧化性越强;
C.同周期原子序数越大,半径越小;
D.主族元素的最高正化合价等于其族序数.
解答 解:A.金属性:Na>Mg>Al,元素的金属性越强,对应的单质的还原性越强,所以还原性:Na>Mg>Al,故A正确;
B.非金属性:Cl>Br>I,元素的非金属性越强,对应单质的氧化性越强,所以氧化性:Cl2>Br2>I2,故B正确;
C.C、N、O原子序数依次增大,所以半径:O<N<C,故C错误;
D.P、S、Cl分别属于第V、VI、VII主族,最高正价分别为+5、+6、+7,故D正确;
故选:C.
点评 本题考查元素非金属性、金属性的递变规律,明确元素在周期表中的位置及元素周期律即可解答,难度不大.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| 金属(粉末状)mol | 酸的浓度及体积 | 反应温度 | |
| A | Zn 0.1 | 6mol/L硝酸 10mL | 70℃ |
| B | Zn 0.1 | 3mol/L硫酸 10mL | 70℃ |
| C | Fe 0.1 | 3mol/L盐酸 10mL | 60℃ |
| D | Zn 0.1 | 3mol/L盐酸 10mL | 60℃ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:丙>乙>甲>丁 | |
| B. | 气态氢化物的熔点:丙>甲 | |
| C. | 乙元素在自然界中形成的化合物种类最多 | |
| D. | 乙和甲、丙、丁都一定能形成两种或两种以上的共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油的催化重整和煤的干馏均可以得到芳香烃,说明石油和煤中含有芳香烃 | |
| B. | 石油裂解的目的主要是为了得到更多的汽油 | |
| C. | 石油分馏得到的产物可用来萃取溴水中的溴 | |
| D. | 石油裂化主要得到的是乙烯、丙烯等 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Na+、SO42-、NO3- | B. | K+、Na+、HCO3-、NO3- | ||
| C. | OH-、HCO3-、Ba2+、Na+ | D. | H+、Fe2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
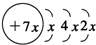 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: ,这样排布遵循了泡利原理和洪特规则.
,这样排布遵循了泡利原理和洪特规则. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12C和C60属于同一种元素,互为同素异形体 | |
| B. | 16O和18O是不同的核素,互为同位素 | |
| C. | 37Cl和35Cl可以通过化学变化实现相互转化 | |
| D. | H2O和H2O2由同种元素组成,二者互为同素异形体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com