
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
下列有关电池的说法不正确的是( )
A.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
B.手机上用的锂离子电池属于二次电池
C.甲醇燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
查看答案和解析>>
科目:高中化学 来源: 题型:
纯碱和小苏打是厨房中两种常见用品,下列区分它们的说法中正确的是( )
|
| A. | 分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打 |
|
| B. | 用洁净铁丝蘸取两种样品在煤气灯火焰上灼烧,使火焰颜色发生明显变化的是小苏打 |
|
| C. | 用两只试管,分别加入少量两种样品,再加入等浓度食醋,产生气泡速率较快的是小苏打 |
|
| D. | 将两种样品配成溶液,分别加入石灰水,无白色沉淀生成的是小苏打 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
A.铝投入氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑
B.氯气与水反应:Cl2 + H2O = 2H+ + Cl- + ClO -
C.碳酸氢钠溶液与少量石灰水反应:2HCO3- + Ca2+ + 2OH- = CaCO3↓+ CO32- + 2H2O
D.单质铜与稀硝酸反应:Cu +2H+ +2NO3- = Cu2+ + 2NO↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关微粒或物质的“量”的叙述不正确的是( )
| A.浓度分别为2mol/L和1mol/L的Na2CO3溶液中,C(CO32-)的比值为2:1 |
| B.常温常压下,16g 02和O3混合气体中含有NA个氧原子 |
| C.46gNO2和N204混合气体的物质的量之和大于O.5mol,小于lmol |
| D.向饱和CuS04溶液中加入1 mol CuS04固体,则析出的晶体的质量大于250g |
查看答案和解析>>
科目:高中化学 来源: 题型:
在25℃时,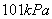 条件下,将
条件下,将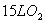 通入10LCO和
通入10LCO和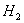 的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和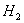 的混合气中V(CO)=__________L,
的混合气中V(CO)=__________L,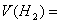 ___________L。
___________L。
(2)若剩余气体的体积是aL,则原CO和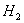 的混合气中
的混合气中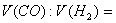 _________。
_________。
(3)若剩余气体的体积是aL,则a的取值范围是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铁单质及其化合物在生产、生活中应用广泛.请回答下列问题:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应式为
________________________________________________________________________.
(2)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是________________________________________________________________________.
(3)硫酸铁可作絮凝剂,常用于净水,其原理是_______________________________
_________________________________________________________(用离子方程式表示).
在使用时发现硫酸铁不能使酸性废水中的悬浮物沉降而除去,其原因是_____________
________________________________________________________________________.
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO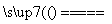 3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是____________.
3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是____________.
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母).
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁的表面能形成致密的氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列家庭化学小实验不能达到预期目的是( )
|
| A. | 用米汤检验食用加碘盐(含KIO3)中含有碘 |
|
| B. | 用醋、石灰水验证蛋壳中含有碳酸盐 |
|
| C. | 用碘酒检验汽油中是否含有不饱和烃 |
|
| D. | 用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸(H2C2O4)是二元弱酸,25℃时,H2C2O4:K1=5.4×10-2,K2=5.4×10-5;H2CO3:K1=4.5×10-7,K2=4.7×10-11。
(1)KHC2O4溶液呈__________性(填“酸”、“中”或“碱”)。
(2)下列化学方程式可能正确的是 。
A.H2C2O4 + CO32- == HCO3- + HC2O4-
B.HC2O4-+ CO32- == HCO3- + C2O42-
C.2C2O42- + CO2 + H2O == 2 HC2O4- + CO32-
D.H2C2O4 + CO32- == C2O42- + CO2↑+ H2O
(3)常温下,向10 mL 0.01 mol·L-1H2C2O4溶液中滴加0.01 mol·L-1的KOH溶液V mL,回答下列问题:
①当V<10时,反应的离子方程式为___________________________________。
②若溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-),则pH______7(填“>”“<”或“=”),V________10(填“>”“<”或“=”)。
③当溶液中离子浓度有如下关系:c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4),则溶液中溶质为____________,V________10(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com