
| A. | △H3=0.33 kJ•mol-1 | |
| B. | 单斜硫转化为正交硫的反应是吸热反应 | |
| C. | 正交硫比单斜硫稳定 | |
| D. | 单斜硫比正交硫稳定 |
分析 A、根据盖斯定律可知,反应①-②=③,所以△H3=(-297.16kJ•mol-1)-(-296.83kJ•mol-1)=-0.33kJ/mol,
B、根据S(单斜,s)═S(正交,s)△H3=-0.33kJ/mol,反应放热;
C、能量高的物质不稳定,能量低的物质稳定;
D、能量高的物质不稳定,能量低的物质稳定.
解答 解:A、由盖斯定律可知,反应①-②=③,所以△H3=(-297.16kJ•mol-1)-(-296.83kJ•mol-1)=-0.33kJ/mol,故A错误;
B、S(单斜,s)═S(正交,s)△H3=-0.33kJ/mol,反应放热,故B错误;
C、根据S(单斜,s)═S(正交,s)△H3=-0.33kJ/mol,单斜硫的能量比正交硫的能量高,正交硫比单斜硫稳定,故C正确;
D、根据S(单斜,s)═S(正交,s)△H3=-0.33kJ/mol,单斜硫的能量比正交硫的能量高,正交硫比单斜硫稳定,故D错误;
故选C.
点评 本题考查化学能与热能,明确盖斯定律计算反应热及物质的能量与稳定性的关系即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①②⑤正确 | B. | 都不正确 | ||
| C. | ④正确,其他不正确 | D. | 仅①不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.56L | B. | 1.12L | C. | 2.24L | D. | 3.36L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学实验小组想要了解市场上食用白醋(主要是醋酸的水溶液)的浓度,采用标准NaOH溶液对某品牌食用白醋进行滴定.
某化学实验小组想要了解市场上食用白醋(主要是醋酸的水溶液)的浓度,采用标准NaOH溶液对某品牌食用白醋进行滴定.| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.32 | 25.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 重金属、农药等会造成水体污染 | |
| B. | 装饰材料中的甲醛、苯等会造成居室污染 | |
| C. | SO2会导致酸雨的形成 | |
| D. | 含磷洗涤剂大量使用易造成水华、赤潮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极为Cu,负极为Fe,电解质溶液为FeCl3 和HCl混合溶液 | |
| B. | 正极为C,负极为Fe,电解质溶液为Fe(NO3)3 和HNO3混合溶液 | |
| C. | 正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3 和H2SO4混合溶液 | |
| D. | 正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3 和HCl混合溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
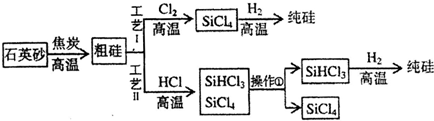
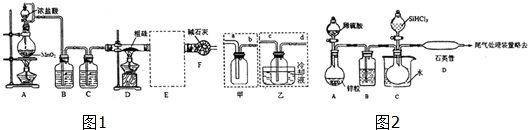
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com