
【题目】下列事实不能用勒夏特列原理(平衡移动原理)解释的是
①溴水中存在化学平衡:Br2+H2O ![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
②铁在潮湿的空气中易生锈
③二氧化氮与四氧化二氮的平衡体系,增大压强后颜色加深
④合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
⑤钠与氯化钾共融制备钾:Na(l)+KCl(l) ![]() K(g)+NaCl(l)
K(g)+NaCl(l)
⑥反应CO(g)+NO2(g) ![]() CO2(g)+NO(g)(正反应为放热反应),达到化学平衡后,升高温度体系的颜色加深
CO2(g)+NO(g)(正反应为放热反应),达到化学平衡后,升高温度体系的颜色加深
A. ①④ B. ②③ C. ②⑥ D. ②③⑥
【答案】B
【解析】
勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动;使用勒夏特列原理时,该反应必须是可逆反应,,否则勒夏特列原理不适用。
①加入AgNO3溶液后, AgNO3和HBr反应导致平衡正向移动,则溶液颜色变浅,能用平衡移动原理解释,故不选;
②铁在潮湿的空气中易生锈是电化学腐蚀,不是可逆反应,故选;
③增大压强,平衡正向移动,气体颜色变浅,但颜色加深是体积缩小,二氧化氮浓度变大,不能用平衡移动原理解释,故选;
④合成氨反应是放热反应,降低温度平衡正向移动,提高氨的产率,故不选;
⑤K为气体,减小生成物的浓度可使平衡正向移动,能用勒夏特列原理解释,故不选;
⑥反应CO(g)+NO2(g) ![]() CO2(g)+NO(g) (正反应为放热反应),达到化学平衡后,升高温度平衡逆向移动,所以二氧化氮的浓度变大,体系的颜色加深,故不选;
CO2(g)+NO(g) (正反应为放热反应),达到化学平衡后,升高温度平衡逆向移动,所以二氧化氮的浓度变大,体系的颜色加深,故不选;
综上分析可知,符合题意的有:②③;本题选B。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是二元弱酸(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀H2C2O4溶液中滴加等浓度NaOH溶液,H2C2O4、HC2O4—、C2O42—的浓度分数δ随溶液pH变化的关系如图,以下说法正确的是( )

A. HC2O4—的浓度分数随pH增大而增大
B. 交点a处对应加入的NaOH溶液的体积为5mL
C. 交点b处c(H+)=6.4×10-5
D. pH=5时存在c(Na+)+c(H+)=c(C2O42—)+c(HC2O4—)+c(OH—)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HI在一定条件下可发生反应 2HI(g) ![]() H2 (g)+I2(g) △H,在2L恒容密闭容器中,充入一定量的 HI(g),反应物的物质的量 n(mol)随时间t(min)变化的数据如下:
H2 (g)+I2(g) △H,在2L恒容密闭容器中,充入一定量的 HI(g),反应物的物质的量 n(mol)随时间t(min)变化的数据如下:

根据表中数据,下列说法正确的是
A. 实验 1中,反应在 0至 10min内,v(HI)=0.02mol·L-1 ·min-1
B. 800℃时,该反应的平衡常数K=0.25
C. 根据实验 1和实验2可说明:反应物浓度越大,反应速率越快
D. △H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰的化合物在工业、医疗等领域有重要应用。某兴趣小组模拟制备KMnO4及探究锰(II)盐能否被氧化为高锰(VII)酸盐。
I.KMnO4的制备:
![]()
反应原理
步骤一:3MnO2+6KOH+KClO3![]() 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O
步骤二:3K2MnO4+2CO2 =2KMnO4+MnO2+2K2CO3
实验操作
步骤一:将一定比例的MnO2、KOH和KClO3 固体混合加热,得到墨绿色的固体,冷却后加水溶解得到碱性K2MnO4溶液放入烧杯C中。
步骤二:连接装置,检查气密性后装药品。打开分液漏斗活塞,当C中溶液完全变为紫红色时,关闭活塞停止反应,分离、提纯获取KMnO4晶体。
装置图如下:

(1)检查装置A气密性:关闭分液漏斗活塞,在B中加入蒸馏水至液面超过长导管口,用热毛巾捂住圆底烧瓶,若__________,则说明装置气密性良好。
(2)B中试剂选择的理由________。
(3)反应结束后,未能及时分离KMnO4晶体,发现C中紫红色溶液变浅。该小组同学认为是碱性K2MnO4溶液中的Cl-将生成的MnO4- 还原,导致颜色变浅,指出含有Cl-的判断依据_____________。
II.该小组继续探究Mn2+能否氧化为MnO4-,进行了下列实验:
装置图 | 试剂X | 实验现象 |
| ① 0.5mL 0.1mol/LNaOH溶液 | 生成浅棕色沉淀,一段时间后变为棕黑色 |
②0.5mL 0.1mol/LNaOH 和15%H2O2 混合液 | 立即生成棕黑色沉淀 | |
③ 0.5mL 0.1mol/LHNO3溶液 | 无明显现象 | |
④ 0.5mL 0.1 mol/LHNO3溶液和少量PbO2 | 滴加HNO3无明显现象,加入PbO2立即变为紫红色,稍后紫红色消失,生成棕黑色沉淀 |
已知:i.MnO2为棕黑色固体,难溶于水;
iiKMnO4在酸性环境下缓慢分解产生MnO2。
(4)实验①中生成棕黑色沉淀可能的原因_____。
(5)实验②中迅速生成棕黑色沉淀的离子方程式_____。
(6)对比实验③和④,实验③的作用_____。
(7)甲同学猜测实验④中紫红色消失的原因:酸性条件下KMnO4不稳定,分解产生了MnO2,乙认为不成立,理由是________;乙认为是溶液中的Mn2+将MnO4- 还原,并设计了实验方案证明此推测成立,其方案为_________。
探究结果:酸性条件下下,某些强氧化剂可以将Mn2+氧化为MnO4-。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,在催化剂a(或催化剂b)存在下,CO2和H2能同时发生两个平行反应,反应的热化学方程式如下:
① CO2(g)+ 3H2(g)![]() CH3OH(g)+ H2O(g) ΔH1= - 53.7 kJ/mol
CH3OH(g)+ H2O(g) ΔH1= - 53.7 kJ/mol
② CO2(g)+ H2(g)![]() CO(g)+ H2O(g) ΔH2= + 41.2 kJ/mol
CO(g)+ H2O(g) ΔH2= + 41.2 kJ/mol
某实验小组控制CO2和H2初始投料比为1∶2.2。在相同压强下,经过相同反应时间测得的实验数据如下:
实验编号 | T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
1 | 543 | 催化剂a | 12.3 | 42.3 |
2 | 543 | 催化剂b | 10.9 | 72.7 |
3 | 553 | 催化剂a | 15.3 | 39.1 |
4 | 553 | 催化剂b | 12.0 | 71.6 |
(备注)甲醇选择性:转化的CO2中生成甲醇的百分比。
下列说法不正确的是
A. 相同温度下,在该时刻催化剂b对CO2转化成CH3OH有较高的选择性
B. 其他条件不变,升高温度反应①中CO2转化为CH3OH平衡转化率增大
C. 其他条件不变,增大反应体系压强反应②中平衡常数不变
D. 反应①在无催化剂、有催化剂a和有催化剂b三种情况下能量示意图如下:

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组制备焦亚硫酸钠(Na2S2O5)并探究其性质。
资料:焦亚硫酸钠为白色晶体;可溶于水。
(1)制备Na2S2O5(夹持装置略)

① A为SO2发生装置,A中反应方程式是_____________________________________。
② B 中析出白色晶体,可采取的分离方法是___________________。
③ 将尾气处理装置C补充完整并标明所用试剂。___________________
(2) 探究Na2S2O5的性质
实验编号 | 实验操作及现象 |
实验Ⅰ | 取B中少量白色晶体于试管中,加入适量蒸馏水,得溶液a,测得溶液呈酸性。 |
实验Ⅱ | 取少量溶液a于试管中,滴加足量氢氧化钡溶液,有白色沉淀生成,过滤后,将沉淀放入试管中,滴加过量盐酸,充分振荡,产生气泡,白色沉淀溶解。 |
实验III | 取B中少量白色晶体于试管中,滴加1mL 2 mol / L酸性KMnO4溶液,剧烈反应,溶液紫红色很快褪去 。 |
实验IV | 取B中少量白色晶体于大试管中加热,将产生的气体通入品红溶液中,红色褪去;将褪色后的溶液加热,红色恢复。 |
① 由实验Ⅰ可知,Na2S2O5溶于水,溶液呈酸性的原因_______________________________________(用化学方程式表示) 。
② 实验Ⅱ中白色沉淀滴加过量盐酸,沉淀溶解,用平衡原理解释原因______________________。
③ 实验III中经测定溶液中产生Mn2+,该反应的离子方程式是_________________________。
④ 实验IV 中产生的气体为____________,实验中利用该气体的_________ 性质进行检验。
⑤ 从上述实验探究中,体现出Na2S2O5具有 _____________________性质。 ( 至少说出两点 )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
下列判断不正确的是
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=![]() mol/L
mol/L
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是( )
A.Cl2能与大多数金属化合,生成高价金属氯化物
B.新制氯水中加入AgNO3溶液,有白色沉淀生成
C.欲除去Cl2中的大量HCl气体,可将此混合气体通过盛有饱和食盐水的洗气瓶
D.漂白粉的有效成分是CaCl2和Ca(ClO)2,应密封保存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一容积不变的密闭容器中充入一定量A(g)和B,发生反应:xA(g)+2B(s) ![]() yC(g) △H<0.在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。
yC(g) △H<0.在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。
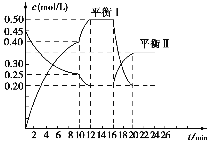
请回答下列问题
(1)根据图示可确定x:y=________。
(2)0-10min容器内压强______ (填“变大”、“ 不变”或“变小”)
(3)推测第10min引起曲线变化的反应条件可能是______(填编号,下同);第16min引起曲线变化的反应条件可能是________。
①减压 ② 增大A的浓度 ③增大C的量 ④升温 ⑤ 降温⑥ 加催化剂
(4)若平衡1的平衡常数为K1,平衡II的平衡常数为K2,则K1______(填“>”“=”或“<”)K2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com