
����Ŀ��ͼ�У�AΪһ����ѧ��ѧ�г����ĵ��ʣ�B��C��D��E�Ǻ���AԪ�صij�����������ǵ���ɫʵ���Ϊ��ɫ��
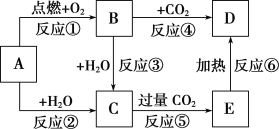
��1��д���������ʵĻ�ѧʽ��B___��
��2������6����Ӧ������������ԭ��Ӧ����___(��д���)��
��3��д��A ��C��Ӧ�����ӷ���ʽ___��
��4��д��B��C��Ӧ�����ӷ���ʽ��___��E��D�Ļ�ѧ����ʽ��___��
��5������5.00gD��E�Ĺ������ʹE��ȫ�ֽ⣬�������������������0.31g����ԭ�������D����������Ϊ___��
���𰸡�Na2O2 �٢ڢۢ� 2Na+2H2O=2Na++2OH-+H2�� 2Na2O2��2H2O��4Na����4OH����O2�� 2NaHCO3![]() Na2CO3��CO2����H2O 83.2%
Na2CO3��CO2����H2O 83.2%
��������
AΪһ����ѧ��ѧ�г����ĵ��ʣ���ɫʵ��Ϊ��ɫ����AΪNa��Na��������ȼʱ���ɹ������ƣ���BΪNa2O2�����������������̼��Ӧ����̼���ƣ���DΪ̼���ƣ�Na��ˮ��Ӧ����C����CΪNaOH��NaOH������Ķ�����̼��Ӧ����̼�����ơ�
��1��������֪��BΪ�������ƣ���ѧʽΪNa2O2��
��2��Na��ˮ��������Ӧʱ�����ϼ۷����ı䣬Ϊ������ԭ��Ӧ�����������������̼��ˮ��Ӧ���ɵ������������ϼ۸ı䣬Ϊ������ԭ��Ӧ��NaOH�������̼��̼����������̼���ƻ��ϼ�δ�䣬Ϊ��������ԭ��Ӧ��
��3��A ��C�ֱ�ΪNa��NaOH��Na��ˮ��Ӧ�����������ƺ����������ӷ���ʽΪ2Na+2H2O=2Na++2OH-+H2����
��4������������ˮ��Ӧ�����������ƺ����������ӷ���ʽΪ2Na2O2��2H2O��4Na����4OH����O2����̼���������ȷֽ�����̼���ơ�������̼��ˮ������ʽΪ2NaHCO3![]() Na2CO3��CO2����H2O��
Na2CO3��CO2����H2O��
��5�����ݷ���ʽ���ٵ�����Ϊ1��1��CO2��H2O����n��NaHCO3��=2n��CO2��=![]() =0.005mol��2��m��NaHCO3��=0.010mol��84g/mol=0.84g��m��Na2CO3��=5.00g-0.84g=4.16g��Na2CO3��������Ϊ
=0.005mol��2��m��NaHCO3��=0.010mol��84g/mol=0.84g��m��Na2CO3��=5.00g-0.84g=4.16g��Na2CO3��������Ϊ![]() ��100%=83.2%��
��100%=83.2%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(GaN)����Ϊ�������뵼���������Ӧ���Ѿ�ȡ����ͻ���ԵĽ�չ��
��֪����i�������������ȶ�������ˮ���ᷴӦ��ֻ�ڼ���ʱ����Ũ����
��ii��NiCl2 ��Һ�ڼ���ʱ����ת��ΪNi(OH)2����ֽ�ΪNiO��
��iii���Ʊ������صķ�ӦΪ��2Ga+2NH3![]() 2GaN+3H2
2GaN+3H2
ijѧУ��ѧ��ȤС��ʵ�����Ʊ������������ʵ��װ����ͼ��ʾ��

���ʵ�鲽��������
���μӼ���NiCl2 ��Һ��ʪ�����ط�ĩ�����ڷ�Ӧ���ڡ�
����ͨ��һ��ʱ����H2���ټ��ȡ�
��ֹͣͨ��������ͨ�백������������һ��ʱ�䡣
��ֹͣ����������ͨ�백��,ֱ����ȴ��
������Ӧ���ڵĹ���ת�Ƶ�ʢ��������ձ��У���ַ�Ӧ���ˡ�ϴ�ӡ����
��1������X�е��Լ���___________������Y��������__________________��
��2��ָ������װ���д���һ�����ԵĴ�����________________________��
��3����������ѡ��NiCl2 ��Һ����ѡ����������ԭ����____________________��
a.����Ӵ�������ӿ컯ѧ��Ӧ����
bʹ���ܾ��ȸ������ط۵ı��棬��ߴ�Ч��
c.Ϊ���ܸ����γ�ԭ��أ��ӿ췴Ӧ����
��4�����������Ʊ������أ����жϸ÷�Ӧ�ӽ����ʱ�۲쵽��������____________________��
��5����д���������м����Ʒ�����ع���ϴ�Ӹɾ��IJ���________________________��
��6����Ԫ������ͬ�壬�������������ƣ���д��������������NaOH��Һ�����ӷ���ʽ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���![]() ��˵����ȷ����
��˵����ȷ����
A. ����̼ԭ�ӿ��ܹ�ƽ�� B. ���������̼ԭ�ӹ�ֱ��
C. ���ֻ��4��̼ԭ�ӹ�ƽ�� D. ���ֻ��3��̼ԭ�ӹ�ֱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ� ��
A.��֪NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ��H=-57.3kJ/mol����ϡ��ˮ��ϡ���ᷴӦ����1molˮʱ���ų�������С��57.3kJ
B.��֪25�棬101kPaʱ��������ȼ����Ϊ285.8kJ/mol��������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��H2(g)+![]() O2(g)=H2O(g) ��H=-285.8kJ/mol
O2(g)=H2O(g) ��H=-285.8kJ/mol
C.��֪25�棬101kPaʱ��ʯī��ȼ����Ϊ393.5kJ/mol����ʯīȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��C+O2=CO2 ��H=-393.5kJ/mol
D.Mg��CO2��ȼ������MgO��C���÷�Ӧ�л�ѧ��ȫ��ת��Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��������й�Cu�����ᡢ���ữѧ���ʵ�ʵ�飬ʵ�������ͼ��ʾ�������й�˵����ȷ����
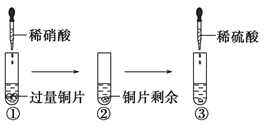
A.ʵ������Թܿ��к���ɫ���������˵��ϡ���ᱻCu��ԭΪNO2
B.ʵ����еμ�ϡ���ᣬͭƬ�����ܽ⣬˵��ϡ����������Ա�ϡ����ǿ
C.������ʵ��ɵó����ۣ�Cu�ڳ����¼ȿ�����ϡ���ᷴӦ��Ҳ������ϡ���ᷴӦ
D.ʵ��۷�����Ӧ�Ļ�ѧ����ʽΪ��3Cu��Cu(NO3)2��4H2SO4 =4CuSO4��2NO����4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E����ǰ������ԭ�������������������Ԫ�ء�A��Dͬ�����������ֳ���������DA2��DA3����ҵ�ϵ������C2A3��ȡ����C��B��E��������ֻ��2�������⣬�������ȫ������Eλ��Ԫ�����ڱ���ds�����ش��������⣺
��1��B��C�е�һ�����ܽϴ���� ______����̬Dԭ�Ӽ۵��ӵĹ������ʽΪ______��
��2��DA2���ӵ�VSEPRģ���� ______��H2A��H2D�ۡ��е�ߵö��ԭ���� ______��
��3��ʵ����C����Ԫ���γɻ������ʵ�����ΪC2Cl6�������ģ����ͼ��ʾ����֪C2Cl6 �ڼ���ʱ���������������NaOH��Һ��Ӧ������Na[C(OH)4]��
![]()
�� C2Cl6����_____���壨������ͣ�������Cԭ�ӵ��ӻ��������Ϊ_____�ӻ���
�� [C(OH)4]���д��ڵĻ�ѧ����___________��
��4����ҵ���Ʊ�B�ĵ����ǵ������B���Ȼ�������ǵ��BA��ԭ����________��
��5��B��C�ķ����ᄃ���ֱܷ���2957 kJ��mol��1��5492 kJ��mol��1���������ܴ��ԭ����_______
��6��D��E���γɻ����ᄃ��ľ�����ͼ��ʾ���ڸþ����У�E����λ��Ϊ___________��
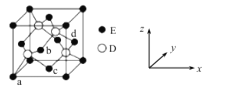
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ��ͨ��������Ӧ����������黹�ܴ������ڵ���
A.������̼��K+��Na+��CO32����Cl��
B.������Ba2+��Mg2+��NO3����Br��
C.�Ȼ��⣺Ca2+��Fe3+��NO3����Cl��
D.��������Na+��NH4+��HCO3����MnO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ����ˮ�ʼ��վ����480 mL 0.5 mol��L-1NaOH��Һ�Ա�ʹ�á�


(1)��ͬѧӦѡ��____mL������ƿ��
(2)�����������ͼ��ʾ������ͼ���в���Ӧ��ͼ��__________ (��ѡ����ĸ)֮�䡣
A.����ۡ�������B.����ڡ�������C.�����
(3)��ͬѧӦ��ȡNaOH����____g��������Ϊ23.1 g���ձ�����������ƽ�ϳ�ȡ����NaOH����ʱ�����ڸ�����ѡȡ����������С____(����ĸ)��������ͼ��ѡ������ȷ��ʾ����λ�õ�ѡ��____(����ĸ)��
���� ������
a | b | c | d | e | |
�����С/g | 100 | 50 | 20 | 10 | 5 |

(4)���в�����������Һ��Ũ�ȴ�С�к�Ӱ��(�ƫ�� ��ƫС������Ӱ�족����
�ٶ���ʱ�����Ӷ�����Ũ�Ȼ�________����ת����Һ�����У�����Һ�彦������Ũ�Ȼ�____________��
������ƿδ���Ũ�Ȼ�__________��
�ܶ���ҡ�Ⱥ�����Һ������ڿ̶��ߣ�Ũ�Ȼ�______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���X��Y����Ϊ������ɡ��������ҩ�����ɡ�������֧�żܣ�δ��ʾ��ԭ�ӻ�ԭ���ŵĿռ����У�
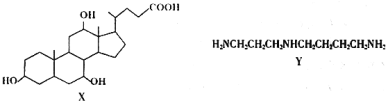
��������������ǣ�������
A.X�ķ���ʽΪ![]()
B.1mol X��Ũ���������·�����ȥ��Ӧ,�������3 mol ![]()
C.X��HBr�ķ�ӦΪ��ȥ��Ӧ
D.Y����ķ��������ʾ����,��Y�ļ��Խ�ǿ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com