
【题目】化合物H是一种著名的香料,某研究小组从苯出发,经两条路线合成化合物H。其中化合物D的分子式为C7H8 。
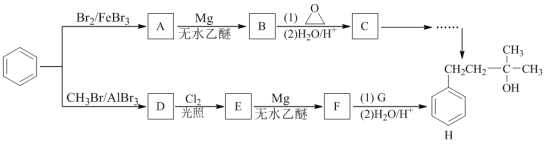
已知:I. RX+Mg无水乙醇R-MgX (X为卤素原子)
II. ![]()
III. 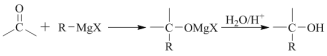
请回答:
(1)下列说法不正确的是________________________。
A.常温下,化合物A为褐色、密度比水大的液体
B.化合物C能发生消去反应
C.化合物D的一氯代物有4种
D.化合物E能发生水解反应和消去反应
(2)苯→D的化学方程式是___________________________________________。
(3)G的结构简式是_______________________________________。
(4)写出同时符合下列条件的C的所有同分异构体的结构简式________________________。
①能与FeCl3溶液发生显色反应;
②1H-NMR谱显示分子中含有四种不同环境的氢原子。
(5)设计以C和丙酮为原料制备H的合成路线(用流程图表示,无机试剂任选,且不超过四步)。_____
【答案】AD ![]()
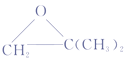
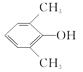 和
和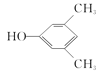
【解析】
根据从苯出发合成H的第一条路线,根据反应条件顺推可知,A为![]() ;结合已知信息中的反应条件顺推可知B为
;结合已知信息中的反应条件顺推可知B为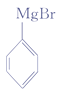 ;C为
;C为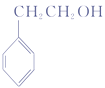 ;根据从苯出发合成H的第二条路线,根据反应条件顺推可知,D为
;根据从苯出发合成H的第二条路线,根据反应条件顺推可知,D为![]() ;E为
;E为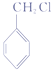 ;F为
;F为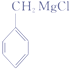 ;F到G增加了4个碳原子,根据G和H的结构特点以及反应条件,顺推可知G为
;F到G增加了4个碳原子,根据G和H的结构特点以及反应条件,顺推可知G为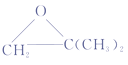 。
。
(1)A.常温下,化合物A(![]() )为无色油状、密度比水大的液体,选项A不正确;
)为无色油状、密度比水大的液体,选项A不正确;
B.化合物C为 ,能发生消去反应生成苯乙烯,选项B正确;
,能发生消去反应生成苯乙烯,选项B正确;
C.化合物D为![]() ,分子中有四种不同环境的氢原子,其一氯代物有4种,选项C正确;
,分子中有四种不同环境的氢原子,其一氯代物有4种,选项C正确;
D.化合物E为 ,在氢氧化钠的水溶液中能发生水解反应生成苯甲醇,但不能发生消去反应,选项D不正确;
,在氢氧化钠的水溶液中能发生水解反应生成苯甲醇,但不能发生消去反应,选项D不正确;
答案选AD;
(2)苯→D是苯与一溴甲烷发生取代反应生成甲苯和溴化氢,反应的化学方程式是![]() ;
;
(3)G的结构简式是 ;
;
(4) C为 ,其同分异构体,根据限定条件①能与FeCl3溶液发生显色反应可知存在酚羟基,根据限定条件②1H-NMR谱显示分子中含有四种不同环境的氢原子,可推出符合条件的同分异构体为
,其同分异构体,根据限定条件①能与FeCl3溶液发生显色反应可知存在酚羟基,根据限定条件②1H-NMR谱显示分子中含有四种不同环境的氢原子,可推出符合条件的同分异构体为 和
和 ;
;
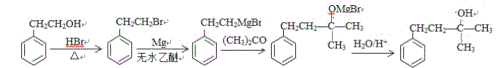
(5)C为 ,与HBr反应制得
,与HBr反应制得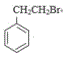 ,
, 在镁和无水乙醚中作用生成
在镁和无水乙醚中作用生成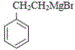 ,
, 与丙酮反应生成
与丙酮反应生成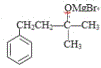 ,
, 酸化得到H的合成路线为
酸化得到H的合成路线为 。
。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,CO和CO2的混合气体共28L,质量为51g。其中CO2的质量为_____g,混合气体中CO的物质的量分数为____。混合气体的平均摩尔质量为_______。
(2)同温同压下,同质量的NH3和H2S气体体积比为______,原子个数之比为______,密度之比为________。
(3)在120℃时分别进行如下四个反应(除S外其它物质均为气体):
A.2H2S+O2=2H2O+2S↓ B.2H2S+3O2=2H2O+2SO2
C.C2H4+3O2=2H2O+2CO2 D.C4H8+6O2=4H2O+4CO2
若反应在压强恒定、容积可变的容器内进行,反应前后气体密度(d)和气体体积(V)分别符合关系式d前>d后和V前<V后的是___________;符合d前>d后和V前>V后的是___________(填写反应的代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图。
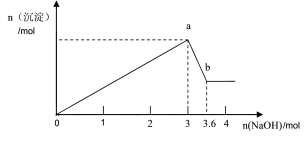
(1)a点对应的沉淀为________________(填化学式)。
(2)计算原混合液中FeCl3的物质的量浓度为多少_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X中仅可能含有K+、Na+、Fe2+、Fe3+、SO42-、CO32-、I-、Cl-中的一种或多种,且溶液中各离子浓度相同。现进行下列实验,下列说法正确的是( )
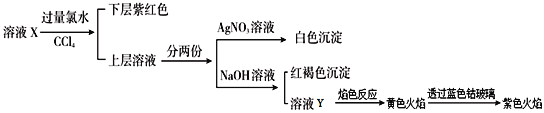
A. 该溶液X中Na+、Cl-一定有
B. 溶液Y中加入氯化钡溶液没有沉淀
C. 该溶液可能是硫酸亚铁、碘化钾和氯化钠溶于水后得到的
D. 原溶液X中滴加几滴KSCN溶液后,再滴加少量的次氯酸钠溶液后溶液呈血红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
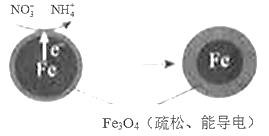
①作负极的物质是____。
②正极的电极反应式是____。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是____。
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用试纸检验气体是一种重要的实验方法。下列试纸的选用以及对应的现象、结论都正确的一项是( )
A. 用干燥的pH试纸检验HCl气体![]()
B. SO2能使湿润的品红试纸褪色
C. 用干燥的红色石蕊试纸检验NH3
D. 能使湿润的淀粉碘化钾试纸变蓝的气体一定是氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。

①作负极的物质是____。
②正极的电极反应式是____。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是____。
(4)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂严重影响人体健康,化合物E是一种临床治疗高血脂症的药物。E的合成路线如下(部分反应条件和试剂略):

请回答下列问题:
(1)试剂Ⅰ的名称是___a___,试剂Ⅱ中官能团的名称是___b___,第② 步的反应类型是____c___。
(2)第①步反应的化学方程式是_____________。
(3)第⑥步反应的化学方程式是_____________。
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,其结构简式是_________ 。
(5)C的同分异构体在酸性条件下水解,生成X、Y和CH3(CH2)4OH。若X含有羧基和苯环,且X和Y的核磁共振氢谱都只有两种类型的吸收峰,则X与Y发生缩聚反应所得缩聚物的结构简式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是三种常见的化合物,A为淡黄色固体,甲是一种金属单质。它们之间的转化关系如图所示:完成下列空白:
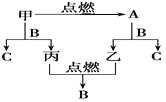
(1)A的化学式:________,B的化学式:________。
(2)写出甲+B反应生成C+丙的化学方程式:_______________________________
(3)写出A的一种重要用途:___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com