
| A. | 次氯酸的结构式:H-Cl-O | |
| B. | 在BF3、PCl5中各元素的最外层都满足8电子稳定结构 | |
| C. | 溴化钙的电子式为:Ca2+[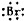 ]${\;}_{2}^{-}$ ]${\;}_{2}^{-}$ | |
| D. | 1molNa2O2中含有3NA个离子(NA表示阿伏加德罗常数) |
分析 A.次氯酸的中心原子为O原子,分子中不存在H-Cl键;
B.B、P原子最外层没有达到8电子稳定结构;
C.两个溴离子不能合并,应该写在钙离子的两边;
D.过氧化钠的化学式中含有2个钠离子和1个过氧根离子.
解答 解:A.次氯酸分子中含有1个H-O键和1个O-Cl键,其正确的结构简式为:H-O-Cl,故A错误;
B.BF3分子中B原子最外层电子数为3+3=6,PCl5分子中P原子最外层电子数为5+5=10,不满足8电子结构,故B错误;
C.溴化钙的电子式中,钙离子直接用离子符号表示,两个溴离子分别标出所带电荷及最外层电子,其正确的电子式为 ,故C错误;
,故C错误;
D.1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总共含有3mol离子,含有离子数为3NA,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法判断,题目难度中等,涉及结构简式、电子式等知识,明确常见化学用语的书写原则为解答关键,注意掌握过氧化钠的化学式组成,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 符合通式CnH2n+2(n≥1)且相对分子质量不相等的有机物为同系物 | |
| B. | 符合同一通式且相对分子质量不相等的有机物为同系物 | |
| C. | 乙醇和甲醚不是同系物但是同分异构体 | |
| D. | CH3CH2CHO、CH2═CHCH2OH、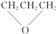 三种物质互为同分异构体 三种物质互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
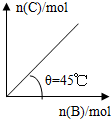
| A. | 平衡时B的转化率为40% | |
| B. | 若再通入B,则再次达平衡时C的体积分数增大 | |
| C. | 在容器中加入催化剂,则B的转化率增大 | |
| D. | 若保持压强一定,当温度升高时,图中θ>45° |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 活化能的大小对化前后的能量变化不产生影响 | |
| B. | 化学键的断裂和形成是物质在化学变化中发生能量变化的主要原因 | |
| C. | 盐酸和NaOH(aq)反应的中和热△H=-57.3kJ.mol-1,则H2S04(aq)和Ba(0H)2(aq)反应的中 和热△H=2×(-57.3 )kJ•mol-1 | |
| D. | 因 N2(g)+3H2(g)?2NHs(g)△H=-dkJ.mol-1,故在某溶器中投入 l molN2与 3molH2充分反应后,放出热量小于dkJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
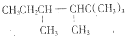 f.C8H10O2
f.C8H10O2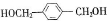 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
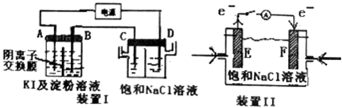 以下装置中,电极材料均为惰性电极.装置Ⅰ中,接通电源,发现A电极附近溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO${\;}_{3}^{-}$+5I-+3H2O.
以下装置中,电极材料均为惰性电极.装置Ⅰ中,接通电源,发现A电极附近溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-=IO${\;}_{3}^{-}$+5I-+3H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com