
【题目】G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的分子式(或化学式),但知道它们在一定条件下具有如下的转换关系(未配平):(1)G→Q+NaCl (2)Q+H2O![]() X+H2 (3)Y+NaOH→G+Q+H2O (4)Z+NaOH→Q+X+H2O这五种化合物中氯的化合价由低到高的顺序为
X+H2 (3)Y+NaOH→G+Q+H2O (4)Z+NaOH→Q+X+H2O这五种化合物中氯的化合价由低到高的顺序为
A. Q、G、Z、Y、X B. G、Y、Q、Z、X
C. G、Y、Z、Q、X D. Z、X、G、Y、Q
 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源: 题型:
【题目】现有含有少量NaCl、 Na2SO4、Na2CO3等杂质的NaNO3溶液,选择适当的试剂除去杂质,得到纯净的NaNO3固体,实验流程如下图所示。
(1)沉淀A的主要成分是、(填化学式)。
(2)①②③中均进行的分离操作是。
(3)溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是 , 为了除去杂质,可向溶液3中加入适量的。
(4)实验探究小组在实验中需要用到456 mL1 molL-1的HNO3溶液,但是在实验室中只发现一瓶8 molL-1的HNO3溶液,该小组用8molL-1的HNO3溶液配制所需溶液。
①实验中所需的玻璃仪器包括、mL量筒、烧杯、、胶头滴管等。
②该实验中需要量取8molL-1的HNO3溶液mL。
③下列实验操作中导致配制的溶液浓度偏高的是。
A.取8molL-1的HNO3溶液溶液时仰视刻度线
B.量取用的量筒水洗后未进行任何操作
C. 8molL-1的HNO3溶液从量筒转移至烧杯后用水洗涤量筒并全部转移至烧杯
D.定容时仰视刻度线
E.定容后,将容量瓶振荡摇匀后,发现液面低于刻度线,未进行任何操作
(5)某同学转移溶液的操作如图所示,该同学操作中的错误是。容量瓶的刻度线标在比较细的瓶颈之上的原因是。
A.为了美观 B.为了统一标准 C.为了提高准确度 D.方便刻画
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用芳香烃X和烯烃Y可以合成紫外线吸收剂BAD. 已知:G不能发生银镜反应,B遇FeCl3溶液显紫色,C到D的过程为引入羧基(﹣COOH)的反应.其中BAD结构简式为: 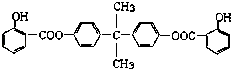
BAD的合成路线如下: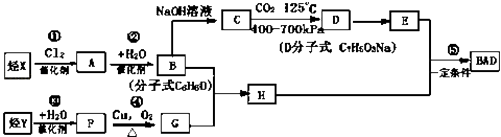
试回答下列问题:
(1)写出结构简式YD .
(2)属于加成反应的有(填数字序号) .
(3)1molBAD最多可与含molNaOH的溶液完全反应.
(4)写出方程式反应④ . F+E .
(5)E有多种同分异构体,判断符合下列要求的同分异构体数目为种. ①能发生银镜反应②遇FeCl3溶液显紫色③核磁共振氢谱图中有四个吸收峰.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中, HCl 作氧化剂的是( )
A. NaOH+HCl=NaCl+H2O
B. Zn+2HCl=ZnCl2+H2↑
C. MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D. CuO+2HCl=CuCl2+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1mol/L
B. 从1L 2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L
C. 配制500mL 0.1mol/L的CuSO4溶液,需8.0g硫酸铜固体
D. 0.1mol/L MgCl2溶液中Cl-物质的量为0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是:
A. 工业上是通过电解氯化铝、氯化镁制备金属铝和镁的
B. 石油经过减压分馏主要得到C5 ~ C11的汽油制品
C. 将重油经过催化裂化可以获取汽油等产品
D. 有机玻璃是将普通硅酸盐玻璃中加入一些有机物混合而成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质A~K有如下的转化关系,其中D,E为气体单质,试回答(图中有些反应的产物和反应的条件没有全部标出): 
(1)写出下列物质的化学式:D是 , G是;
(2)写出“C→F”反应的离子方程式;
(3)写出反应“F→G”的离子方程式;
(4)写出反应“I→J”的离子方程式;
(5)在溶液I中滴入NaOH溶液,可观察到的现象是;写出相关的化学反应方程式 .
(6)向200mL 3mol/L溶液J中加入60g铁、铜混合物(铁和铜的物质的量比为1:1),充分反应后过滤,向滤液中通入足量的氨气,充分反应后再过滤、洗涤、干燥、灼烧,灼烧后得到固体的质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性条件下,向硫酸锰(MnSO4)溶液中滴加高碘酸钾(KIO4)溶液,溶液颜色会变为紫红色,生成高锰酸钾(KMnO4).试完成下列相关题目:
(1)该反应的氧化剂是 , 反应中MnSO4表现性.
(2)由题意可知,KIO4和KMnO4二者相比,的氧化性强.
(3)若20mL0.003mol/L MnSO4溶液与15mL0.01mol/L KIO4溶液可以恰好反应,则该反应中KIO4对应的产物是(填字母)A KI B I2 C KIO2 D KIO3
依据你的判断,请写出该反应的离子方程式,并配平:
(4)将下列所给物质的化学计量数填在横线上,并用单线桥法标明电子转移的方向和数目.
MnSO4+KIO4+…
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com