
【题目】在下列反应中, HCl 作氧化剂的是( )
A. NaOH+HCl=NaCl+H2O
B. Zn+2HCl=ZnCl2+H2↑
C. MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D. CuO+2HCl=CuCl2+H2O
科目:高中化学 来源: 题型:
【题目】下列溶液中物质的量浓度为1mol/L的是
A.将40gNaOH 溶解在1L水中
B.将22.4LHCl气体溶于水配成1 L溶液
C.将1L 10 mol/L的浓盐酸加入9 L水中
D.将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠和铯都是碱金属元素,下列关于铯及其化合物的叙述中正确的是
A. 铯的密度比水小,像钠一样浮在水面上
B. 铯与水反应十分剧烈,甚至会发生爆炸
C. 碳酸铯加热时易分解成二氧化碳和氧化铯
D. 氢氧化铯是强碱,其碱性比氢氧化钾弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2的含量是空气质量日报中一项重要检测指标,请结合所学知识回答下列问题.
(1)工业制硫酸过程中,SO2催化氧化的原理为: 2SO2(g)+O2(g) ![]() 2SO3(g)
2SO3(g)
T℃时,向某密闭容器中充入一定SO2(g)和O2(g),发生上述反应,测得SO2(g)的平衡转化率(a)与体系总压强(p)的关系如图1所示.
①a、b两点对应的平衡常数K(a)K(b)(填“>”、“<”或“=”,下同),SO2浓度c(a)c(b).
②c点时,反应速率v(正)v(逆) .
(2)电化学法处理SO2 . 硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如图2所示(电极均为惰性材料):
①M极发生的电极反应式为 .
②若使该装置的电流强度达到2.0A,理论上每分钟应向负极通入标准状况下气体的体积为L(已知:1个e﹣所带电量为1.6×10﹣19C).
(3)溶液法处理SO2 . 已知常温下H2SO3和H2CO3的电离常数如表所示:
电离常数 | K1 | K2 |
H2SO3 | 1.3×10﹣2 | 6.3×10﹣8 |
H2CO3 | 4.2×10﹣7 | 5.6×10﹣11 |
常温下,将SO2缓慢通入100mL 0.2molL﹣1的Na2CO3溶液中,当通入448mLSO2时(已折算为标准状况下的体积,下同),发生的离子方程式为;当通入896mLSO2时,所得溶液呈弱酸性,溶液中各离子浓度由大到小的顺序为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图1所示.已知 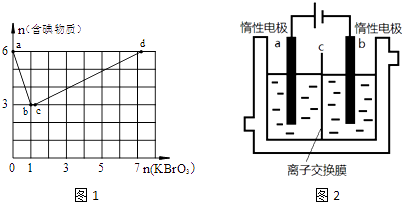
①BrO3﹣+6I一+6H+=3I2+Br﹣+3H2O;
②2BrO3﹣+I2=2IO3﹣+Br2;
请回答下列问题:
(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为 , 还原产物是 .
(2)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式 .
(3)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确,并说明理由 .
(4)含6mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为 .
(5)加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图2所示.先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解.阳极的电极反应式为;阴极观察到的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的分子式(或化学式),但知道它们在一定条件下具有如下的转换关系(未配平):(1)G→Q+NaCl (2)Q+H2O![]() X+H2 (3)Y+NaOH→G+Q+H2O (4)Z+NaOH→Q+X+H2O这五种化合物中氯的化合价由低到高的顺序为
X+H2 (3)Y+NaOH→G+Q+H2O (4)Z+NaOH→Q+X+H2O这五种化合物中氯的化合价由低到高的顺序为
A. Q、G、Z、Y、X B. G、Y、Q、Z、X
C. G、Y、Z、Q、X D. Z、X、G、Y、Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. CaCO3+2HCl=CaCl2+CO2↑+ H2O
B. CaO+H2O=Ca(OH)2
C. 2H2O2![]() 2H2O+O2↑
2H2O+O2↑
D. CaCO3![]() CaO+CO2↑
CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知如下反应,回答下列问题:
3I2 + 6NaOH = 5NaI + NaIO3 + 3H2O
(1)画出这个反应的双线桥___________
(2)_______是氧化剂,氧化产物是___________;
(3)氧化剂与还原剂的物质的量之比为____________,当反应消耗3mol NaOH时,转移的电子数目为_________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com