
【题目】下列有关碳元素的叙述,不正确的是( )
A. 在细胞中,碳元素属于大量元素
B. 碳元素是构成细胞的最基本的元素
C. 碳元素参与生物体内所有化合物的组成
D. 地球上的生命是在碳元素的基础上建立起来的
科目:高中化学 来源: 题型:
【题目】卤族元素是非常重要的非金属元素,其单质和化合物有广泛用途,化学性质也非常丰富。
(1)基态氯原子的价电子排布式为__________________,其核外电子占据的最高能层的符号是_________。
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是___________。
(3)ClO2—的立体结构为_______形,中心氯原子的杂化轨道类型为_________,写出ClO2—一个等电子体的化学式 ______。
(4)下列分子中只存在s-p![]() 键的是_____________。
键的是_____________。
A. H2 B.F2 C.HCl D.HClO
(5)CsICl2不稳定,受热时可能按下列两种方式分解,已知生成物晶格能越大反应越易发生,则CsICl2按下列______方式分解更合理。
A.CsICl2=CsI+Cl2 B. CsICl2=CsCl+ICl
(6)由F、K、Mg三种元素形成的某离子晶体的晶胞结构如下图所示,晶胞边长为a nm(1nm=10—9m)。
①该晶体的化学式为___________________。
②该晶体的密度为____________gcm—3。(结果保留1位小数)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在25 mL0.1mol/L的NaOH溶液中,逐滴加入0.2 mol/L的CH3COOH溶液,溶液的pH与CH3COOH 溶液体积关系如图所示。下列有关粒子浓度关系正确的是

A. 曲线上A、B间的任意一点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. B点:c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C. C点:c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D. D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习与研究化学经常要进行实验,请完成以下课题:
(1)玻璃棒的作用主要有以下三种,请回答下列问题: a.搅拌 b.引流 c.蘸取溶液
①实验室配制一定物质的量浓度溶液,将固体溶解时,玻璃棒的作用是(填字母),
②将烧杯中的溶液注入容量瓶时,玻璃棒的作用是(填字母),
③用浓盐酸检验氨气时,玻璃棒的作用是(填字母),
④粗盐提纯时,用过滤的方法除去不溶性的泥沙,玻璃棒的作用是(填字母).
(2)现用98%的浓H2SO4(ρ)=1.84g/cm3)配制浓度为0.5mol/L的稀硫酸500mL. ①选用的玻璃仪器除了量筒、玻璃棒、烧杯,还用到、 .
②将浓H2SO4沿烧杯内壁慢慢注入盛水的烧杯中,不断搅拌的目的是 , 若搅拌过程中有液体溅出,会使最终结果(填“偏高”、“偏低”或“无影响”).
③定容时必须使溶液凹液面与刻度线相切,若俯视会使结果(填“偏高”、“偏低”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰干电池在放电时电池总反应方程式为Zn+2MnO2+2NH![]() ===Zn2++Mn2O3+2NH3↑+H2O。在此电池放电时,正极(碳棒)上发生反应的物质是( )
===Zn2++Mn2O3+2NH3↑+H2O。在此电池放电时,正极(碳棒)上发生反应的物质是( )
A. 锌 B. MnO2和NH![]() C. 碳 D. Zn2+和NH3
C. 碳 D. Zn2+和NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。常温时,H2S在水中的电离常数Ka1=1.3×10-7,Ka2=7.0×10-15。按要求回答下列问题:
(1)H2S在水中的二级电离常数表达式Ka2=______;0.1mol/LNa2S溶液中离子浓度由大到小的顺序为__________.
(2)常温下,向0.1mol/LH2S溶液中通入HCl或加入NaOH固体,测得c(S2-)与溶液pH的关系如图(忽略溶液体积的变化及H2S的挥发)。

①当溶液中c(S2-)=1.4×10-19mol/L时,溶液中c(OH-)=______,水电离产生的c(H+)=______.
②当pH=13时,溶液中的c(H2S)+c(HS-)=_______.
(3)在工业废水处理中常用H2S将Mn2+转化为MnS除去。常温下,向含有0.010mol·L-1 Mn2+废水中通入H2S以调节废水的pH,当c(HS-)=2.0×10-4mol·L-1时,Mn2+开始沉淀,此时废水的pH=___。[已知Ksp(MnS)=1.4×10-15]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的结构(键线式)及球棍模型如图1:该有机分子的核磁共振氢谱图如图2(单位是ppm):下列关于该有机物的叙述正确的是( ) 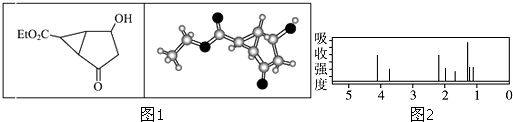
A.该有机物不同化学环境的氢原子有6种
B.该有机物属于芳香化合物
C.键线式中的Et代表的基团为﹣CH3
D.该有机物在一定条件下能够发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是人类从海水资源获取某些重要化工原料的流程示意图:
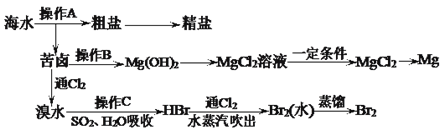
回答下列问题:
(1)操作A是___________和过滤(填实验基本操作名称)。
(2)操作B需加入下列试剂中的一种,最合适的是______(选填编号)。
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳 d.碳酸钠溶液
(3)工业上由无水MgCl2制取镁的化学方程式为__________________________________。
(4)0.25 mol Cl2缓慢通入含有0.1 mol FeBr2、0.1 mol FeI2的混合溶液中,充分反应,试用一个离子方程式表示总反应:__________________________________________。
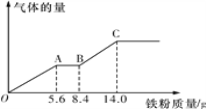
(5)某稀硫酸和稀硝酸的混合溶液100 mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。则原混合溶液中NO3-的物质的量为__________,硫酸的物质的量浓度为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com