
【题目】实验室制取乙烯并检验乙烯性质的装置如下图。

请回答有关问题:
(1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是_________________;
(2)烧瓶中产生乙烯的反应方程式为:_________________,反应类型为:_________________;C中发生反应的化学方程式为:_________________,反应类型为:_________________;
(3)反应一段时间后,可观察到D中的现象是:_________________;
(4)B中所装的溶液是:_________________溶液,起的作用是_________________。
【答案】(1)防止暴沸 (2)CH3CH2OH![]() CH2=CH2↑+H2O 消去反应
CH2=CH2↑+H2O 消去反应
Br2+CH2=CH2→BrCH2CH2Br;加成反应 (3)酸性高锰酸钾溶液褪色 (4)NaOH;除去制取乙烯气体产生的杂质SO2和CO2等,避免影响乙烯的性质检验
【解析】
试题分析:(1)反应条件是加热到170℃,因乙醇的沸点低,易暴沸,在圆底烧瓶中放2-3块碎瓷片的目的是防止暴沸;
(2)利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生消去反应,所以实验室制取乙烯的化学方程式为CH3CH2OH![]() CH2=CH2↑+H2O,乙烯含有碳碳双键,能和溴发生加成反应Br2+CH2=CH2→BrCH2CH2Br,生成1,2-二溴乙烷褪色;
CH2=CH2↑+H2O,乙烯含有碳碳双键,能和溴发生加成反应Br2+CH2=CH2→BrCH2CH2Br,生成1,2-二溴乙烷褪色;
(3)乙烯分子中含有碳碳双键,能使酸性高锰酸钾溶液褪色,因此反应一段时间后,可观察到D中的现象是:酸性高锰酸钾溶液褪色;(4)反应中挥发出的乙醇、乙酸和其它副产物气体(如乙醚、SO2和CO2等),干扰检验乙烯性质实验,因此可用10%的NaOH溶液吸收。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】(1)某科研小组研究:在恒温、恒容(容器容积为2L,)下N2(g)+3H2(g)![]() 2NH3(g)反应的变化。初始条件n (H2)= 3mol 、n (N2)=1mol,反应达到平衡时H2的转化率为60%,NH3的体积分数约为43%
2NH3(g)反应的变化。初始条件n (H2)= 3mol 、n (N2)=1mol,反应达到平衡时H2的转化率为60%,NH3的体积分数约为43%
①此条件下反应的平衡常数K= 。
②若初始条件n (NH3)= 2mol,反应达到平衡时NH3的转化率为 ,
③若初始条件n (H2)= 6mol 、n (N2) =2mol,反应达到平衡时NH3的体积分数 43%,此时移除0.5 mol NH3 ,再次达到平衡时NH3的体积分数 43% (填 “>、<、=”)
(2)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g)![]() 4NO2(g)+O2(g),ΔH>0
4NO2(g)+O2(g),ΔH>0
①下表为该反应在T1温度下的部分实验数据
t/s | 0 | 500 | 1000 |
c(N2O5)/mol·L—1 | 5.00 | 3.52 | 2.48 |
则500s内NO2的平均生成速率为 。
②现以NO2、O2、N2O5、熔融盐NaNO3组成的燃料电池,采用电解法制备N2O5,装置如图所示。

写出石墨I电极上发生反应的电极反应式 。
在电解池中生成N2O5的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是 ( )
A.4.6g由NO2和N2O4组成的混合物中氧原子总数为0.2NA
B.标准状况下,22.4L的SO3中含3NA个氧原子。
C.100mL18.4mol/L的浓硫酸与足量的铜加热反应,转移的电子数为1.84NA
D.密闭的容器中,催化剂作用下0.5molN2与1.5molH2反应后得到NH3分子数一定为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼及其化合物在工业上有许多用途。工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5H2O和Fe3O4。
(1)基态铁原子的外围电子层排布为_____________,该元素位于元素周期表中的第_____________族,在水溶液中常以Fe2+、Fe3+的形式存在,其中_____________更稳定。
(2)以硼酸为原料可制得NaBH4,B原子的杂化方式为_____________。
(3)第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中不正确的是( )

A.分子中5个R﹣Cl键键能不都相同
B.键角(Cl﹣R﹣Cl)有90°、120、180°几种
C.RCl5受热后会分解生成分子立体结构呈三角锥形的RCl3
D.每个原子都达到8电子稳定结构
(4)因为氯化铝易升华,其双聚物Al2Cl6结构如图1所示。1mol该分子中含__________个配位键,该分子________(填“是”或“否”)平面型分子。

(5)纯叠氮酸(HN3)在常温下是一种液体,沸点较高,为308.8 K,主要原因是_________。
(6)二硫化碳属于_________(填“极性”或“非极性”)分子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol分子式为CmHn的有机化合物在氧气中完全燃烧,且生成CO2和H2O的物质的量相等,并消耗168L氧气。(体积均在标准状况下测定);
(1)该有机化合物的分子式。
(2)若分子中只有两个甲基且属于不饱和烃,写出其结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A可发生如下转化(方框内物质均为有机物,部分无机产物已略去):

已知: (R、R'可表示烃基或官能团)
(R、R'可表示烃基或官能团)
请回答:
(1)F蒸气密度是相同条件下H2密度的31倍,且分子中无甲基。已知1 mol F与足量钠作用产生H2 22.4 L(标准状况),则F的分子式是__________________。
(2)G与F的相对分子质量之差为4,则G的性质是________(填字母)。
a.可与银氨溶液反应 b.可与乙酸发生酯化反应
c.可与氢气发生加成反应 d.1 mol G可与2 mol新制Cu(OH)2发生反应
(3)D能与NaHCO3反应,且两分子D可以反应得到含有六元环的酯类化合物,E可使溴的四氯化碳溶液褪色,则D→E的化学方程式是_______________________
(4)B的同分异构体较多,写出一种不含甲基能发生银镜反应的同分异构体结构简式:_________。
(5)A转化为B和F的化学方程式是_________________________。
(6)某烃分子H的碳原子数小于10,核磁共振氢谱只有一组峰, 在相同条件下也可发生类似B → C的反应并只生成一种有机物I,I的结构简式: _______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氯化亚铁的熔点674℃、沸点1023℃;三氯化铁在300℃以上易升华,易溶于水并且有强烈的吸水性。在500℃条件下氯化亚铁与氧气可能发生多种反应,反应之一为:12FeCl2 +3O2![]() 2Fe2O3 +8FeCl3。某研究小组选用以下装置(夹持装置省略,装置可重复选用)进行反应的探究。回答下列问题:
2Fe2O3 +8FeCl3。某研究小组选用以下装置(夹持装置省略,装置可重复选用)进行反应的探究。回答下列问题:


(1)装置的合理连接顺序为A、 、D,其中E装置U形管左边设计为粗导管的目的是 。
(2)A装置中发生反应的化学方程式为 。
(3)反应过程发现,装置B中除生成红棕色固体外,还观察到黄绿色气体,生成该气体的化学方程式为 。
(4)待B中充分反应后,停止加热后,还需持续通氧气至 。
(5)设计实验:
①利用E装置U形管里的固体验证Fe(OH)3是弱碱: 。
②测定装置B的残留固体中铁元素的质量分数: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加罗常数的值,下列有关叙述正确的个数为
①1mol苯乙烯中含有的碳碳双键数为4NA
②4.2g乙烯和丙烯混合气中含有的极性键数目为0.6NA
③标况下,3.36LHF含有的电子数为1.5NA
④常温下1L 0.5mol/L NH4Cl溶液与2L 0.25mol/L NH4Cl溶液所含NH4+的数目相同
⑤常温下4.6gNO2和N2O4混合气体中所含原子总数为0.3NA
⑥在KClO3+6HCl(浓)=KCl+3Cl2+3H2O反应中,每生成1mol Cl2转移的电子总数为2 NA
⑦1mol铁粉在1mol氯气中充分燃烧,失去的电子数为3NA
⑧高温下,16.8g Fe与足量水蒸气完全反应失去0.8NA个电子.
A.3个 B.4个 C.5个 D.6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围有碳粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH(难溶于水),回收处理该废电池可以得到多种化工原料,有关数据下图所示:
溶解度/(g/100g水)
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
①普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH。该电池中,负极材料主要是________,正极发生的主要反应式是 。
加碱调节溶液pH,使溶液中氢氧根离子浓度达到 mol/L,铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全)。继续加碱调节pH为 ,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。
(2)在分析化学中常用Na2C2O4晶体(溶液无色)作为基准物质测定KMnO4溶液的浓度。在H2SO4溶液中,反应如下:2MnO+5C2O+16H+![]() 2Mn2+(溶液无色)+10CO2↑+8H2O。
2Mn2+(溶液无色)+10CO2↑+8H2O。
①若将W g Na2C2O4配成100 mL标准溶液,移取20.00 mL置于锥形瓶中,则酸性KMnO4溶液应装在__________(填“酸式”或“碱式”)滴定管中。本次滴定 选择指示剂(填“需要”、“不需要”)。判断滴定达终点的现象是____ ___。
②若滴定管起始读数和终点读数如图所示,则酸性KMnO4的物质的量浓度为_ (填表达式)。
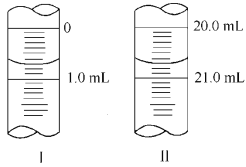
③若滴定完毕立即读数,测定的KMnO4溶液的浓度___(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com