
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是 ( )
A.4.6g由NO2和N2O4组成的混合物中氧原子总数为0.2NA
B.标准状况下,22.4L的SO3中含3NA个氧原子。
C.100mL18.4mol/L的浓硫酸与足量的铜加热反应,转移的电子数为1.84NA
D.密闭的容器中,催化剂作用下0.5molN2与1.5molH2反应后得到NH3分子数一定为NA
【答案】A
【解析】
试题分析:A.NO2和N2O4的最简式均为NO2,所以4.6g由NO2和N2O4组成的混合物中NO2部分的物质的量为4.6g÷46g/mol=0.1mol,氧原子总数为0.2NA,A项正确;B.在标准状况下,三氧化硫是固体,无法通过气体摩尔体积计算物质的量,B项错误;C.根据化学反应Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O 转移2e-,若浓硫酸完全反应,转移的电子数为1.84NA,实际上,铜与稀硫酸不反应,所以转移的电子数小于1.84NA,C项错误;D.工业合成氨是可逆反应,所以密闭的容器中,催化剂作用下0.5molN2与1.5molH2反应后得到NH3分子数小于NA,D项错误;答案选A。
CuSO4+SO2↑+2H2O 转移2e-,若浓硫酸完全反应,转移的电子数为1.84NA,实际上,铜与稀硫酸不反应,所以转移的电子数小于1.84NA,C项错误;D.工业合成氨是可逆反应,所以密闭的容器中,催化剂作用下0.5molN2与1.5molH2反应后得到NH3分子数小于NA,D项错误;答案选A。


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】
物质的结构决定物质的性质。请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有_________种。
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_________________。
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是_____________,1mol(C2H5O)3P=O分子中含有的σ键的数目为__________________。
(4)已知固态NH3、H2O、HF的氢键键能和结构如下:


解释H2O、HF、NH3沸点依次降低的原因___________________。
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有___________个,与碳原子等距离最近的碳原子有__________个。已知碳化硅晶胞边长为apm,则晶胞图中1号硅原子和2号碳原子之间的距离为________pm,碳化硅的密度为__________g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是人类生活中继铜、铁之后又一个重要的金属。工业上冶炼金属铝的原料来源于自然界中重要的矿物质钒土(主要成分:Al2O3;还有SiO2、Fe2O3、FeCO3、MgCO3等杂质)。从钒土中提取得到Al2O3的工艺流程如下图所示:

请回答下列问题:
(1)固体A所含物质的化学式(或分子式)是 。
(2)写出溶液A与足量气体B反应的离子方程式 。
(3)工业冶炼金属铝通常用石墨碳块作电解槽的阳极,请你根据电解原理解释电解冶炼铝的过程中,需要定期补充阳极碳块的原因 。
(4)Al2O3的熔点很高,因而在工业冶炼时,需将Al2O3熔于熔化的冰晶石(Na3AlF6)中进行电解。请写出电解过程中阴极的电极反应式 。工业上通常将Al(OH)3和Na2CO3一同溶于氢氟酸来制取冰晶石,反应时放出CO2气体,写出该反应的化学方程式 。
(5)有一位同学查阅资料发现,AlCl3的熔点很低。他提出:可通过电解熔融状态的AlCl3制取金属铝。你认为他提出的方案是否可行?为什么? 。
(6)某企业用上述工艺流程进行生产,每10.0t钒土可得到金属铝1.35t。如果不考虑生产过程的损耗,请你计算钒土中Al2O3的质量分数 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图有机物分子中带“※”碳原子是手性碳原子(连有四个不同基团的碳原子)。该有机物分别发生下列反应,生成的有机物分子中不会含有手性碳原子的是( )

①与甲酸发生酯化反应
②与足量NaOH水溶液反应
③与银氨溶液作用只发生银镜反应
④催化剂作用下与H2反应
A. ①②③④ B. ①③
C. ②④ D. 以上反应都不成立
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向体积恒定为2 L的密闭容器里充入2 mol M和一定量的N,发生如下反应:M(g)+N(g)![]() E(g)。当反应进行到4min时达到平衡,测得M的浓度为0.2 mol·L-1。下列说法正确的是( )
E(g)。当反应进行到4min时达到平衡,测得M的浓度为0.2 mol·L-1。下列说法正确的是( )
A.4min时,M的转化率为80%
B.4min时,用M表示的反应速率为0.8mol·L-1·min-1
C.4min后,向容器中充入不参与反应的稀有气体,M的物质的量减小
D.2min时,M的物质的量浓度为0.6mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示氮及其化合物在一定条件下的转化关系:

(1)① 反应II的化学方程式是______。
② 反应II其中一步反应为2NH3 (g)+3Cl2(g) =N2 (g) +6HCl(g) ΔH=–462 kJmol-1
已知:![]()
![]()
断开1 mol H–N键与断开1 mol H–Cl键所需能量相差约为_______ kJ。
(2)反应III是利用右图所示装置电解制备NCl3(氯的化合价为+1),其原理是:NH4Cl+2HCl![]() NCl3 +3H2↑。
NCl3 +3H2↑。

① b接电源的_______极(填“正”或“负”)。
② 阳极反应式是_______。
(3)反应III得到的NCl3可以和NaClO2制备 ClO2,同时生成NH3,该反应的离子方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯的同系物是人类最早认识的芳香族化合物,其中对二甲苯(英文名称p—xylene,缩写为PX)是化学工业的重要原料。
已知: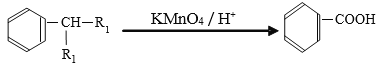
(1)写出PX的结构简式______________。
(2)PX可能发生的反应有__________、_____________。(填反应类型,只填两种。)
(3)有机物M存在如下图所示的转化关系,其中A 是PX的一种同分异构体。

已知:M的分子式为C16H22O4,D能发生银镜反应。
①B的苯环上存在3 种不同化学环境的氢原子,则B 的结构简式是__________。
②D分子中所含的官能团是______________(填化学式)。
③M的结构简式是_______________。
(4)F是B的一种同分异构体,具有如下特征:
a.是苯的对位二取代物; b.遇FeCl3溶液显示紫色; c.能与碳酸氢钠溶液反应。
写出F与NaHCO3溶液反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙烯并检验乙烯性质的装置如下图。

请回答有关问题:
(1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是_________________;
(2)烧瓶中产生乙烯的反应方程式为:_________________,反应类型为:_________________;C中发生反应的化学方程式为:_________________,反应类型为:_________________;
(3)反应一段时间后,可观察到D中的现象是:_________________;
(4)B中所装的溶液是:_________________溶液,起的作用是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验题:绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下列是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法。

已知:室温下饱和 H2S溶液的 pH 约为3.9,SnS沉淀完全时溶液的 pH 为1.6;FeS开始沉淀时溶液的 pH 为3.0,沉淀完全时的 pH 为5.5。
(1) 操作Ⅱ,在溶液中用硫酸酸化至 pH=2的目的是_______________________。
(2)操作Ⅳ的顺序依次为________、________、过滤、洗涤、干燥。
(3)操作Ⅳ得到的绿矾晶体用少量冰水洗涤,其目的是:
①除去晶体表面附着的硫酸等杂质;
②________________________________________________________________________。
(4)测定绿矾产品中Fe2+含量的方法是
a.称取一定质量的绿矾产品,配制成250.00 mL溶液;
b.量取25.00 mL 待测溶液于锥形瓶中;
c.用硫酸酸化的 0.010 00 mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00 mL。
滴定时发生反应的离子方程式为5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O
①用硫酸酸化的 0.010 00 mol·L-1 KMnO4溶液滴定时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化判断此滴定实验达到终点的方法是___________________;
②若用上述方法测定的样品中FeSO4·7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有___ _。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com